ブリッジレポート:(7776)セルシード vol.14
| (7776:JASDAQ) セルシード |
|
||||||||
|
||||||||
企業名 |
株式会社セルシード |
||
社長 |
長谷川 幸雄 |
||
所在地 |
東京都新宿区原町3-61 桂ビル4F |
||
決算期 |
12月末日 |
業種 |
精密機器(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2013年12月 | 105 | -534 | -581 | -584 |
| 2012年12月 | 75 | -846 | -842 | -913 |
| 2011年12月 | 86 | -1,418 | -1,358 | -1,442 |
| 2010年12月 | 66 | -1,204 | -1,002 | -1,009 |
| 2009年12月 | 87 | -785 | -788 | -790 |
| 2008年12月 | 61 | -778 | -644 | -650 |
| 2007年12月 | 40 | -809 | -614 | -616 |
| 2006年12月 | 23 | -672 | -464 | -470 |
| 2005年12月 | 34 | -412 | -336 | -343 |
| 2004年12月 | 53 | -257 | -214 | -215 |
| 株式情報(2/28現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
【事業内容】
事業は、各種用途向けに様々な種類の細胞シートを開発・製造・販売する「細胞シート再生医療事業」と、細胞シートの培養器材である温度応答性細胞培養器材及びその応用製品の開発・製造・販売を行う「再生医療支援事業」とに分かれる。「細胞シート再生医療事業」では、共同研究先と複数の再生医療医薬品パイプライン(新薬候補)の研究開発を進めている。
・米国角膜再生上皮シート:動物実験が終了し、バイオロジックス(生物学
的製剤)としての認定受領 ・心筋再生パッチ :ヒト骨格筋芽細胞シートの実用化でテルモ社と 基本合意(12年3月発表) ・食道再生上皮シート :共同研究先での臨床研究が終了し良好な結果が 得られた (12年8月発表)他、海外の共同研究 先が臨床研究の準備を進めている。 【同社技術基盤の優位性】
現在、「細胞シート工学」だけが唯一「ヒト細胞のみからの組織の人工作製」という課題を原理的に解決しており、また、角膜再生上皮シート、食道再生シート、心筋再生パッチ、歯周組織再生シート・軟骨再生シートといった様に「細胞シート再生医療」の科学的なProof of Concept が多様な組織・疾患のヒト臨床で示されている。加えて、上市済み再生医療製品の殆どは皮膚と軟骨であり、上記の通り細胞シート再生医療の応用面での多様性は類を見ない。
【事業環境】
再生医療の産業化を取り巻く環境は追い風を受けており、特に安倍政権下で法整備が進んだ日本は再生医療事業環境の活性化が顕著である。例えば、13年4月には再生医療の実用化を目指した再生医療推進法が成立し、同年11月には改正薬事法(いわゆる医薬品医療機器等法)と再生医療等安全性確保法が成立した。医薬品医療機器等法においては、医薬品や医療機器とは別に「再生医療等製品」が新たに定義され、その特性を踏まえた制度(例:条件及び期限付承認制度、いわゆる早期承認制度)が導入された。また、再生医療等安全性確保法においては、再生医療を3つのカテゴリーに分類して安全性確保を図るリスク別安全性規制が導入された他、細胞加工業(特定細胞加工物の製造を外部委託できる仕組み)が新たに創設される事となった。
|
| 2013年12月期の取り組みと進捗状況(中期経営計画:13/12期~15/12期) |
|
(1)中期経営計画(13/12期~15/12期)の策定と推進
13/12期は13年2月に発表した中期経営計画に基づく3つの柱を推進し、新しい成長モデルの構築に取り組んだ。尚、中期経営計画はローリング方式を採用しており、毎期見直しを行う。
中長期ビジョン 外部環境の変化を活用した新たな持続的成長モデルの構築
第1の柱 「事業提携」の実現により、細胞シート再生医療第1号製品の早期事業化を図る
第2の柱 中長期的な企業価値成長を目指した「戦略分野への先行投資」を行う 第3の柱 収支バランスを改善し、持続的成長を支え得る「財務基盤」を確立する 進捗状況
第1の柱 「事業提携」の実現により、細胞シート再生医療第1号製品の早期
事業化を図る ・角膜再生上皮シートに関する開発戦略の組み換え
再生医療産業化へ向けた環境整備が急速に進展した事を踏まえて、同社は日本における開発に重点を置く方針に転換した。具体的には、日本において、事業提携や公的助成・補助等を活用して開発を推進していく考え。一方、欧州では、欧州医薬品庁(EMA)との協議結果及び日本における急速な産業化環境整備などを踏まえて、EMA宛に提出していた販売承認申請を3月に一旦取り下げた。ただ、将来の販売承認取得可能性は確保しており、現在、事業提携による事業化を検討中である。一方、米国では、Emmaus Medical 社と共同で開発・事業化に向けた取り組みが進められている(角膜にフォーカスするため、同社と交わした2本の契約を1本に統合するべく交渉中)。
・角膜再生上皮シートに関する日本での取り組み(経産省委託事業)
平成25年度「再生医療等産業化促進事業」の一環として、「世界標準に向けた角膜再生上皮シートの有効性評価手法」の開発、及び「細胞シート生産自動化導入に最適な品質評価方法」の検証の2つの案件を経済産業省から受託した。前者は海外で受けた再生医療製品薬事審査の実績を踏まえての受託で、後者は再生医療支援事業における同社の経験を踏まえたもの。題材となるパイプラインは自家口腔粘膜上皮細胞シートで、角膜再生上皮シートに関するこれまでの経験・ノウハウが活用できる。加えて、前者の成果は、原料細胞が共通する自家食道再生上皮シートに応用可能であり、後者の成果は、様々なパイプラインの生産自動化(生産コスト低減、品質担保等)に応用が可能だ。実施期間は契約締結日から2014年3月31日。
※参考 「世界標準に向けた角膜再生上皮シートの有効性評価手法」の開発
角膜再生上皮シートの有効性評価手法は、現時点では定性的評価にとどまるが、有効性を定量的に判断できる合理的な評価方法の設定が不可欠である。このため、本事業では有効性の客観的評価が可能な①安定した上皮の回復による視軸上の結膜化の減少及び②角膜血管新生の阻害の打倒性、について検証する。①安定した上皮の回復による視軸上の結膜化の減少の検証では、術後12ヶ月目にフルオレセイン染色試験を実施し、角膜表面に存在する結膜を画像解析により定量的に解析する(ベースライン:移植直後)。また、角膜上皮の回復によって得られる結膜化の抑制を、視軸上の結膜化割合を定量化する事で有効性の判断基準とする。 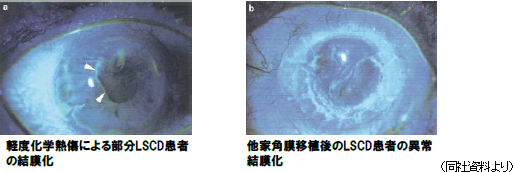  第2の柱 中長期的な企業価値成長を目指した「戦略分野への先行投資」を
13/12期は6件の出願済み特許が成立した。具体的には、新型温度応答性細胞培養器材技術「共培養用器材表面」(欧州、5月発表)、密閉型細胞培養容器による上皮系細胞の新規培養方法(日本、5月発表)、移植用角膜内皮再生シート(韓国、1月発表)、角膜内皮再生シート(韓国、6月発表)、移植用角膜再生シート((米国、10月発表)、及び癌組織モデル作製用癌細胞シート(日本、6月発表)。
行う 第3の柱 収支バランスを改善し、持続的成長を支え得る「財務基盤」を
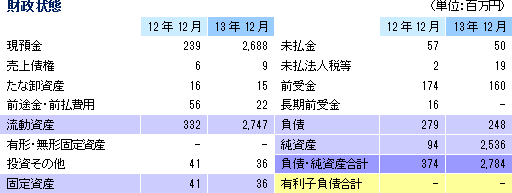
約29億円の資金調達を行い、財務諸表における「継続企業の前提に関する注記」の記載を解消した。
確立する  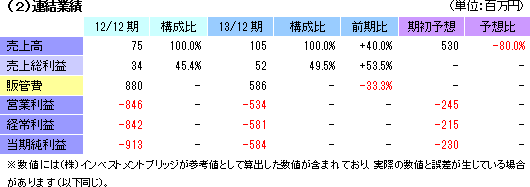 売上高105百万円、経常損失581百万円
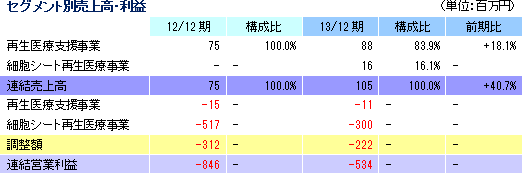
売上高は前年同期比40.0%増の105百万円。内訳は、再生医療支援事業が88百万円(前年同期比13百万円増)、細胞シート再生医療事業が16百万円(前年同期は売上計上無し)。細胞シート再生医療事業では、欧州における角膜再生上皮シート開発計画見直しに伴いGENESIS Pharma SAとの販売提携契約を解消したため、契約締結時に受領した一時金16百万円を売上計上した。営業損失は534百万円(前年同期は846百万円の損失)。経営合理化策に基づく経費削減と研究開発費の抑制(461百万円→228百万円)で販管費が586百万円と同33.3%(293百万円)減少した。 期初予想との差異要因
売上高については、事業提携一時金350百万円が獲得できなかった(提携交渉継続中)事、及び契約の見直しに伴い(交渉継続中)、Emmaus社から受領済みの一時金110百万円の売上高への振り替えができなかった事が下振れ要因。欧州角膜販売提携解消に伴う受領済み一時金(前受金)の売上高振替16百万円や再生医療支援事業売上高18百万円の計上は業績予想に織り込まれていなかったが、下振れ要因に比べると僅少。
営業損益では、売上高の下振れが425百万円の損益悪化要因となる一方、販管費の抑制効果が想定以上に顕在化し149百万円の損益改善要因となった。
   |
| 2014年12月期の取り組み(中期経営計画:14/12期~16/12期) |
|
(1)環境認識
2013年は日本が再生医療の産業化で世界をリードし始める画期的な年となった
「日本の再生医療は、現在、産業化に向けたステージにあり、今後、本格的な成長加速期を迎える」と言うのが同社の考え。国策として再生医療の産業化が進められており、2013年は下記法律の制定・改正が実現し法規整備が進んだ。・ 再生医療推進基本法(昨年4月成立) ・ 改正薬事法(早期承認制度等、昨年11月成立) ・ 再生医療等安全性確保法(加工業等、昨年11月成立) この他、研究開発向け公的補助・助成の拡充や市場創出へ向けた支援に加え、世界で初めてiPS細胞ヒト臨床研究も承認された(7月、網膜治療)。 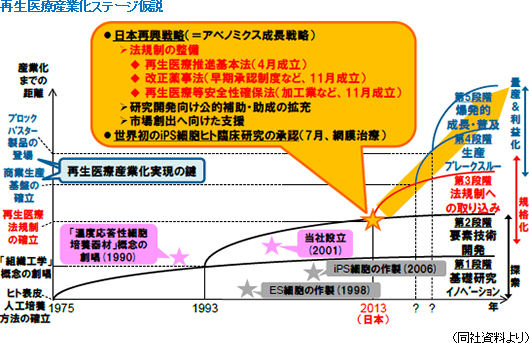 「再生医療産業化」実現のキーワードは3つの“A” (Automation、Allogeneic、Alliance)
再生医療産業化ステージ仮説に基づく今後のキードライバーは、「商業生産基盤の確立」と「ブロックバスター製品の登場」。「商業生産基盤の確立」には、生産コストの抜本的低減、生産能力の飛躍的増強、及び製品品質の向上・均一化が必要不可欠であり、「ブロックバスター製品の登場」のためには、大型市場(例:1,000億円以上/年)の戦略的ターゲティング、オープンイノベーションの活用による差別化&技術課題の解決、及び製品特性に合致した充分量のマーケティング先行投資の投下が必須。また、共に、Automation(生産システムの自動化)、Allogeneic(他家細胞原料化の実現)、Alliance(産学連携・事業提携による取り組み)がキーワードとなる。
細胞シート工学は「ヒト細胞のみからの組織の人工作製」という課題を原理的に解決した画期的技術
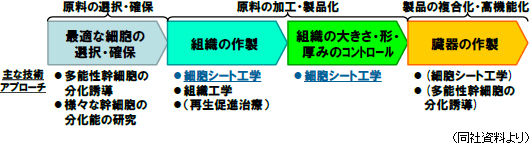
再生医療のプロセスは、最適な細胞の選択・確保 → 組織の作製 → 組織の大きさ・形・厚みのコントロール → 臓器の作製。細胞シート工学は、このプロセスのうち、組織の作製、組織の大きさ・形・厚みのコントロール、及び臓器の作製にアプローチできる技術である。組織の作製プロセスでは、細胞シート工学は 「ヒト細胞のみから様々な種類の組織を人工作製する」という課題を原理的に解決しており、組織の大きさ・形・厚みのコントロールでは、細胞シート工学はこの課題を解決する原理(積層化+血管導入)を非臨床研究で示す事に成功している。一方、臓器の作製は組織作製が出来て初めて取り組む事ができる課題である。
 (2)中期経営計画の概要(14/12期~16/12期)
再生医療本格産業化へのロードマップ :日本で開発した 「再生医療産業化パッケージ」で世界市場の開拓を目指す
「細胞シート工学」という日本発の革新的再生医療技術を基盤として様々な「細胞シート再生医療」製品を開発し、その世界普及を推進するためには、細胞シート再生医療第1号製品を早期に上市する必要がある。同社は産学連携や事業提携を通じて、自家再生医療の実現を図る考え。産学連携や事業提携する事で、事業化に至る先行投資負担の軽減、機能、スキル、技術など同社が比較優位を持たない経営資源を補完していく。また、再生医療の本格産業化(他家原料+生産自動化)に向け、他家再生医療の実現にも取り組む。
中期経営計画(14/12期~16/12期)
概要:13年2月に発表した中期経営計画の「3つの柱」を拡充
「外部環境の変化を活用した新たな持続的成長モデルの構築」という中期的ビジョンの下、3つの柱を推進する。
第1の柱 「事業提携」の実現により、細胞シート再生医療第1号製品の早期事業化
を図る 第2の柱 中長期的な企業価値成長を目指した「戦略分野への先行投資」を行う 第3の柱 収支バランスを改善し、持続的成長を支え得る「財務基盤」を確立する 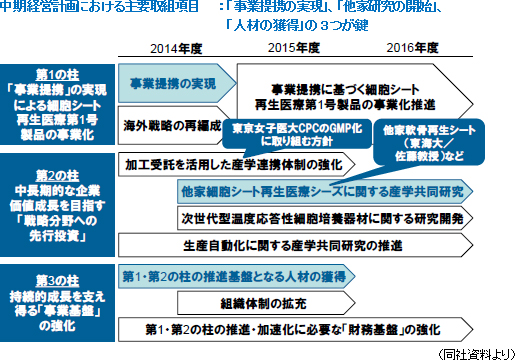  ・現在推進中の事業提携交渉における条件交渉の阻害要因となる可能性 ・研究開発費に関する不確定要素(事業提携の内容に応じて研究開発活動計画が変わる可能性) 尚、上記の再生医療支援事業の予想では、再生医療関連研究開発需要の高まりを受けて、16/12期以降の増収率が年率5%程度で推移すると考えている。 (3)第三者割当による第1回無担保転換社債型新株予約権付社債及び第12回新株予約権の発行による資金調達
第三者割当による第1回無担保転換社債型新株予約権付社債(以下、転換社債)及び第12回新株予約権(以下、新株予約権)の発行により資金調達を行う。この資金調達を通じて戦略的テーマに関する中長期的研究開発活動を加速する事で中長期的な企業価値向上を図る考え。調達額の総額は新株予約権の将来的な行使による概算調達額2,277百万円を含めた2,786百万円。内訳は、第1回無担保転換社債型新株予約権付社債の発行による調達500百万円、第12回新株予約権の発行による調達9百万円、及び将来的な行使による概算調達額2,277百万円。具体的な調達資金の使途は、他家軟骨細胞シートの研究開発を中心とした「戦略投資」資金、研究開発組織体制の強化に必要な人件費、細胞シート再生医療第1号製品の事業化推進資金、及び運転資金への充当。 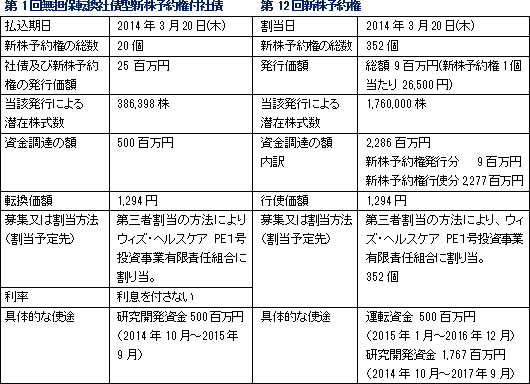 割り当て予定先の選定理由
今回の割当予定先であるウィズ・ヘルスケアPE1号投資事業有限責任組合は、同ファンドの業務執行組合員であるウィズ・パートナーズが創設したファンドであり、ファンド自体は純投資を目的としているものの、ウィズ・パートナーズは、日本におけるバイオベンチャー黎明期である1999年にバイオ・ヘルスケア分野への投資を本格的に開始し、以来、国内外(日本、米国、ドイツ、フランス、イスラエル、韓国等)のバイオ・ヘルスケア分野の投資先30社程度への投資実績を有する。また、経営幹部の専門性について略歴、面談等を通じてバイオ・ヘルスケア産業及び事業経営等に精通している事を確認している事に加え、金融商品取引業者(関東財務局(金商)第2590号)に登録されている事や有利子負債がなく資本も充実している事等から、独立系のファンドとして高い信用と安定した経営基盤を持つ会社であると考えている。加えて、ウィズ・ヘルスケアPE1号投資事業有限責任組合の組成目的は、同組合契約書によれば、「尊い命を守り、より健やかな生活を実現するために、独創的な科学上の発見や技術革新をもとに医薬品開発を進める企業に投資をすること」であり、(株)セルシードの事業内容及び事業方針に合致する。以上を総合的に勘案して、(株)セルシードは同ファンドを割当予定先として選択した。 割り当て予定先の保有方針
割当予定先であるウィズ・ヘルスケアPE1号投資事業有限責任組合は、原則として取得した(株)セルシード株式を中長期保有する意思を有しておらず、市場動向、投資家の需要、提携先の意向等を勘案しながら売却する方針。もっとも、単なる投資の回収を目的として新株式を市場で売却するのではなく、(株)セルシードと事業上のシナジー効果が見込まれる先あるいは安定株主となり得る先への譲渡を可能な限り模索し、資本構成の最適化を通じて、株式市場における評価を高めていく考え。また、ウィズ・パートナーズを通して製薬企業等との業務提携等、(株)セルシードの企業価値向上に資する施策の支援も受ける予定。ただ、ウィズ・ヘルスケアPE1号投資事業有限責任組合は、出資者に対する運用責任を遂行する立場から、市場への影響に十分配慮しつつ、インサイダー取引規制なども考慮した上で、保有株式を市場で売却する可能性はある。 |
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2026 Investment Bridge Co.,Ltd. All Rights Reserved. |




