ブリッジレポート:(7776)セルシード vol.33
| (7776:JASDAQ) セルシード |
|
||||||||
|
||||||||
企業名 |
株式会社セルシード |
||
社長 |
橋本 せつ子 |
||
所在地 |
東京都江東区青海二丁目5番10号 テレコムセンタービル |
||
決算期 |
12月末日 |
業種 |
精密機器(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2017年12月 | 85 | -1,024 | -964 | -966 |
| 2016年12月 | 100 | -1,413 | -1,415 | -1,414 |
| 2015年12月 | 193 | -568 | -531 | -535 |
| 2014年12月 | 86 | -601 | -577 | -582 |
| 2013年12月 | 105 | -534 | -581 | -584 |
| 2012年12月 | 75 | -846 | -842 | -913 |
| 2011年12月 | 86 | -1,418 | -1,358 | -1,442 |
| 2010年12月 | 66 | -1,204 | -1,002 | -1,009 |
| 2009年12月 | 87 | -785 | -788 | -790 |
| 2008年12月 | 61 | -778 | -644 | -650 |
| 2007年12月 | 40 | -809 | -614 | -616 |
| 2006年12月 | 23 | -672 | -464 | -470 |
| 2005年12月 | 34 | -412 | -336 | -343 |
| 2004年12月 | 53 | -257 | -214 | -215 |
| 株式情報(11/13現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
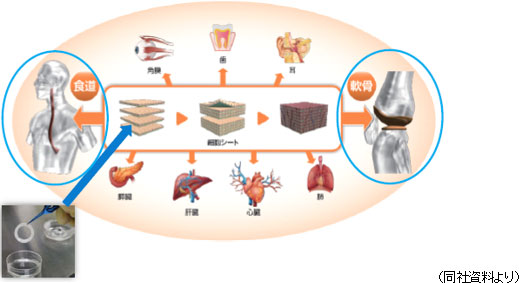
東京女子医科大学の岡野光夫教授が開発した日本発・世界初の「細胞シート工学」を基盤技術とし、この技術に基づいて作製した「細胞シート(シート状の培養細胞)」を用いた再生医療等製品の開発を行う細胞シート再生医療事業と細胞シートの基盤ツール(培養器材)である温度応答性細胞培養器材等の開発・製造・販売及び再生医療の研究開発・事業化を支援する再生医療受託サービスを提供する「再生医療支援事業」を二本柱とする。
細胞シート再生医療事業
大学との共同研究(臨床研究)によりシーズを発掘し事業化する。現在のパイプラインは、「細胞シート工学」を基盤技術とする「食道再生上皮シート」と膝軟骨の「軟骨再生シート」の2本。「食道再生上皮シート」は国内の治験で症例登録が完了し、19/12期中の販売承認申請と承認取得を目指しており、台湾でも提携先が治験届の提出準備を進めている。「軟骨再生シート」も国内で治験開始に向けた準備が進んでいる。ただ、「細胞シート工学」を用いた再生医療製品は、食道や膝軟骨にとどまらない。角膜、歯、耳、肺、心臓、肝臓、及びすい臓の治療でも臨床研究が進められており、既に臨床データも有する。欧州での「歯周組織再生シート」や「食道再生上皮シート」等が次期パイプラインとして検討されている。開発品目や地域についての研究実施機関との契約等、準備が整い次第開発に着手する。
 再生医療支援事業
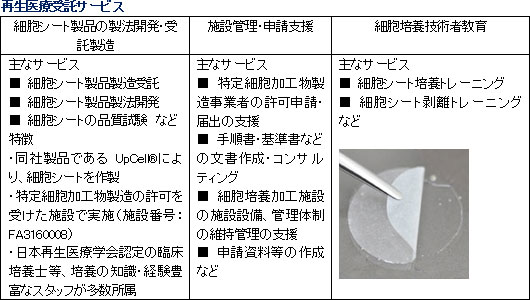
温度応答性細胞培養器材等の開発・製造・販売、及び再生医療に関わる総合的なサポートサービスを提供する再生医療受託サービスを手掛けている。再生医療受託サービスで提供する主なサービスは、細胞シート製品の製法開発・受託製造、運営・申請支援、細胞培養技術者教育等である。 再生医療支援事業
温度応答性細胞培養器材等の開発・製造・販売、及び再生医療に関わる総合的なサポートサービスを提供する再生医療受託サービスを手掛けている。再生医療受託サービスで提供する主なサービスは、細胞シート製品の製法開発・受託製造、運営・申請支援、細胞培養技術者教育等である。
  細胞培養センター
延床面積約763 ㎡で、自動モニタリングシステムによって、清浄度、室圧、温湿度、機器(培養器や保冷庫等)が自動管理され、監視カメラシステムも完備。また、羽田空港まで車で約20分と至近で空輸にも対応しやすい。2017年3月には「再生医療等の安全性の確保等に関する法律第35 条第1項の規定に基づく「特定細胞加工物製造許可」(許認可権者:厚生労働省)を取得しており、特定細胞加工物の受託製造も可能。 細胞培養センター
延床面積約763 ㎡で、自動モニタリングシステムによって、清浄度、室圧、温湿度、機器(培養器や保冷庫等)が自動管理され、監視カメラシステムも完備。また、羽田空港まで車で約20分と至近で空輸にも対応しやすい。2017年3月には「再生医療等の安全性の確保等に関する法律第35 条第1項の規定に基づく「特定細胞加工物製造許可」(許認可権者:厚生労働省)を取得しており、特定細胞加工物の受託製造も可能。
 |
| 2018年12月期第3四半期決算とトピックス |
 台湾事業の進捗で営業損失が大幅に減少
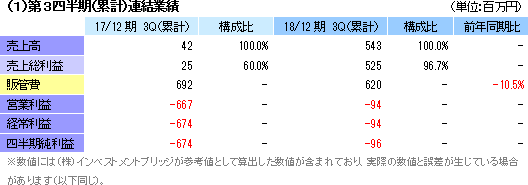
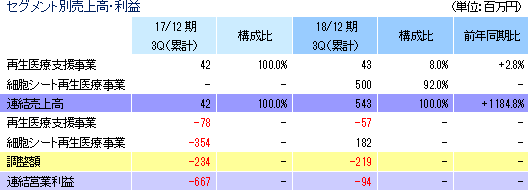
売上面では、細胞シート再生医療事業において、台湾事業の提携先であるMetaTech社への事業提携に係る一時金収入5億円を計上。再生医療支援事業では前年同期(42百万円)とほぼ同水準の43百万円の売上を計上した。
損益面では、売上の増加に伴い売上総利益が大幅に増加する一方、研究開発費(3億66百万円→2億98百万円)を中心に販管費が減少した。また2016年8月から進めてきた食道再生上皮シートの治験の症例登録が4月に完了した。 台湾事業の進捗で営業損失が大幅に減少
売上面では、細胞シート再生医療事業において、台湾事業の提携先であるMetaTech社への事業提携に係る一時金収入5億円を計上。再生医療支援事業では前年同期(42百万円)とほぼ同水準の43百万円の売上を計上した。
損益面では、売上の増加に伴い売上総利益が大幅に増加する一方、研究開発費(3億66百万円→2億98百万円)を中心に販管費が減少した。また2016年8月から進めてきた食道再生上皮シートの治験の症例登録が4月に完了した。
  (2)トピックス
9月に、国立研究開発法人日本医療研究開発機構(以下、「AMED」)が公募した補助事業である平成30年度「再生医療の産業化に向けた評価基盤技術開発事業(再生医療シーズ開発加速支援)」に、同社が提案した研究開発課題「同種軟骨細胞シート(CLS2901C)の製品化に向けた製造方法の確立」が採択された。最長3年程度(2018年10月(予定)~2021年3月)、補助金を受け取りながら、変形性膝関節症の軟骨欠損への適応を目指すヒト(同種)軟骨組織由来細胞シート(CLS2901C)の製品化に向けた製造方法や品質管理試験の最適化、及び安全性試験等の研究開発(データ取得)を進める事ができる。
第4四半期入りした10月11日には同社の細胞培養センター(東京都江東区)が「再生医療等製品製造業許可」を取得した。また、同月18日には、厚生労働省「第76回先進医療技術審査部会」において、同社の共同研究先である東海大学医学部付属病院が申請した「自己細胞シートによる軟骨再生治療」が審議を通過した。今後、厚生労働省先進医療会議での審議を経て正式な承認手続きに進む。 (2)トピックス
9月に、国立研究開発法人日本医療研究開発機構(以下、「AMED」)が公募した補助事業である平成30年度「再生医療の産業化に向けた評価基盤技術開発事業(再生医療シーズ開発加速支援)」に、同社が提案した研究開発課題「同種軟骨細胞シート(CLS2901C)の製品化に向けた製造方法の確立」が採択された。最長3年程度(2018年10月(予定)~2021年3月)、補助金を受け取りながら、変形性膝関節症の軟骨欠損への適応を目指すヒト(同種)軟骨組織由来細胞シート(CLS2901C)の製品化に向けた製造方法や品質管理試験の最適化、及び安全性試験等の研究開発(データ取得)を進める事ができる。
第4四半期入りした10月11日には同社の細胞培養センター(東京都江東区)が「再生医療等製品製造業許可」を取得した。また、同月18日には、厚生労働省「第76回先進医療技術審査部会」において、同社の共同研究先である東海大学医学部付属病院が申請した「自己細胞シートによる軟骨再生治療」が審議を通過した。今後、厚生労働省先進医療会議での審議を経て正式な承認手続きに進む。
|
| 中期経営計画(18/12期~20/12期)と進捗状況 |
 細胞シート再生医療事業では、食道再生上皮シート及び軟骨再生シートの開発に注力していく。食道再生上皮シートは、国内で19/12期中の販売承認取得と販売開始を予定しており、20/12期には販売を本格化させたい考え。また、台湾事業において、細胞シート再生医療事業(食道再生上皮シート・軟骨再生シート)の台湾での独占的な開発・製造・販売権を付与したMetaTech社への開発・製造関連データの提供に伴い、18/12期は10億円程度の対価を受領できる見込み。台湾事業の実績を踏まえ、細胞シート再生医療事業の普及を目指して、アジア諸国・欧米への更なる提携・ライセンシング等を推進していく。これらの取り組みにより、18/12期はセグメント売上高11億円が見込まれる。
再生医療支援事業では、器材製品の海外市場販売戦略の見直しを行い、改めて販売を強化する。また、一部サービスを拡張し、再生医療に関わる総合的なサポートを通じて、再生医療の研究開発・事業化を支援する再生医療受託サービスを開始する。18/12期は器材製品の販売でセグメント売上高70百万円を見込んでおり、19/12期以降、再生医療受託サービスが寄与してくる見込み。
食道再生上皮シートの進捗状況
18/12期第2四半期(2018年4月)に治験の症例登録が完了し、19/12期上期に販売承認申請を行う予定。2017年2月に先駆け審査指定を受けているため販売承認申請から6カ月程度で承認が下りる見込み。このため、19/12期中の販売承認取得と販売開始を予定しており(販売は薬価収載後になる)、20/12期には販売を本格化させたい考え。病院(口腔粘膜採取)→培養施設(細胞をシート状に培養)→病院(細胞シート移植)というサプライチェーンの構築を並行して進めている。
欧州では、スウェーデンでの企業治験を検討しており、その推進役となる子会社CellSeed Sweden AB(スウェーデン)を2015年5月に設立し、2016年には、欧州全体での承認を目指して、欧州医薬品庁(EMA)との相談を開始した。ただ、国内での細胞シート再生医療の事業化を最優先課題とし、欧州での食道再生上皮シート開発については「次期開発品目」の候補品目の一つとして開発優先順位を検討していく方針。
台湾事業は台湾MetaTech社との事業提携の下で進めており、MetaTech社は18/12期中の食道再生上皮シートの治験届提出に向け準備を進めている。18/12期上期に一部開発データの提供が完了し3億25百万円の売上を計上し、第3四半期には1億75百万円を計上した。第4四半期には、更に5億円程度の売上計上が見込まれている。台湾では、台湾版先進医療とも言える細胞治療関連の法改正が進められており(2018年9月施行予定)、対象に同社の軟骨再生シートが含まれる可能性がある。
軟骨再生シートの開発加速
自己細胞(本人の細胞)と同種細胞(他人の細胞)で研究開発を進めており、自己細胞による軟骨再生シートについては、東海大学で8症例の臨床研究の実績があり、先進医療の承認取得に向けた作業が進められている。10月に厚生労働省「第76回先進医療技術審査部会」の審議を通過しており、厚生労働省先進医療会議での審議を経て正式な承認手続きに進む。先進医療申請の結果を踏まえて企業治験が実施される。先進医療として承認されると、公的医療保険の対象外ではあるが、保険診療との併用が認められる。先進医療で使用される細胞シートの受託加工は同社が有償で実施する事が決まっている。
同種細胞による軟骨再生シートについては、2017年2月に東海大学で1症例目の移植手術が実施され、経過は良好。臨床研究として3年間で10名の患者への移植を予定しており、19/12期にかけて続く見込み(2018年上期までに3症例の実績)。この間に、同社は20/12期中の企業治験開始に向け、レギュラトリーサイエンス戦略相談・レギュラトリーサイエンス総合相談及び治験準備を進める。
世界展開に向けた事業提携推進
既契約先であるMetaTech社への支援を推進しつつ、アジア諸国・欧米をターゲットに海外の事業提携先を探索していく。
細胞シート再生医療事業では、食道再生上皮シート及び軟骨再生シートの開発に注力していく。食道再生上皮シートは、国内で19/12期中の販売承認取得と販売開始を予定しており、20/12期には販売を本格化させたい考え。また、台湾事業において、細胞シート再生医療事業(食道再生上皮シート・軟骨再生シート)の台湾での独占的な開発・製造・販売権を付与したMetaTech社への開発・製造関連データの提供に伴い、18/12期は10億円程度の対価を受領できる見込み。台湾事業の実績を踏まえ、細胞シート再生医療事業の普及を目指して、アジア諸国・欧米への更なる提携・ライセンシング等を推進していく。これらの取り組みにより、18/12期はセグメント売上高11億円が見込まれる。
再生医療支援事業では、器材製品の海外市場販売戦略の見直しを行い、改めて販売を強化する。また、一部サービスを拡張し、再生医療に関わる総合的なサポートを通じて、再生医療の研究開発・事業化を支援する再生医療受託サービスを開始する。18/12期は器材製品の販売でセグメント売上高70百万円を見込んでおり、19/12期以降、再生医療受託サービスが寄与してくる見込み。
食道再生上皮シートの進捗状況
18/12期第2四半期(2018年4月)に治験の症例登録が完了し、19/12期上期に販売承認申請を行う予定。2017年2月に先駆け審査指定を受けているため販売承認申請から6カ月程度で承認が下りる見込み。このため、19/12期中の販売承認取得と販売開始を予定しており(販売は薬価収載後になる)、20/12期には販売を本格化させたい考え。病院(口腔粘膜採取)→培養施設(細胞をシート状に培養)→病院(細胞シート移植)というサプライチェーンの構築を並行して進めている。
欧州では、スウェーデンでの企業治験を検討しており、その推進役となる子会社CellSeed Sweden AB(スウェーデン)を2015年5月に設立し、2016年には、欧州全体での承認を目指して、欧州医薬品庁(EMA)との相談を開始した。ただ、国内での細胞シート再生医療の事業化を最優先課題とし、欧州での食道再生上皮シート開発については「次期開発品目」の候補品目の一つとして開発優先順位を検討していく方針。
台湾事業は台湾MetaTech社との事業提携の下で進めており、MetaTech社は18/12期中の食道再生上皮シートの治験届提出に向け準備を進めている。18/12期上期に一部開発データの提供が完了し3億25百万円の売上を計上し、第3四半期には1億75百万円を計上した。第4四半期には、更に5億円程度の売上計上が見込まれている。台湾では、台湾版先進医療とも言える細胞治療関連の法改正が進められており(2018年9月施行予定)、対象に同社の軟骨再生シートが含まれる可能性がある。
軟骨再生シートの開発加速
自己細胞(本人の細胞)と同種細胞(他人の細胞)で研究開発を進めており、自己細胞による軟骨再生シートについては、東海大学で8症例の臨床研究の実績があり、先進医療の承認取得に向けた作業が進められている。10月に厚生労働省「第76回先進医療技術審査部会」の審議を通過しており、厚生労働省先進医療会議での審議を経て正式な承認手続きに進む。先進医療申請の結果を踏まえて企業治験が実施される。先進医療として承認されると、公的医療保険の対象外ではあるが、保険診療との併用が認められる。先進医療で使用される細胞シートの受託加工は同社が有償で実施する事が決まっている。
同種細胞による軟骨再生シートについては、2017年2月に東海大学で1症例目の移植手術が実施され、経過は良好。臨床研究として3年間で10名の患者への移植を予定しており、19/12期にかけて続く見込み(2018年上期までに3症例の実績)。この間に、同社は20/12期中の企業治験開始に向け、レギュラトリーサイエンス戦略相談・レギュラトリーサイエンス総合相談及び治験準備を進める。
世界展開に向けた事業提携推進
既契約先であるMetaTech社への支援を推進しつつ、アジア諸国・欧米をターゲットに海外の事業提携先を探索していく。
 |
|
| <参考:コーポレート・ガバナンスについて> |
 基本的な考え方
当社は、技術革新と創造性を発揮し、質の高い優れた製品とサービスの提供を通じ人々の健康と福祉に貢献していくことを使命とし、全ての企業活動において品質を高めるべく企業統治の整備を進めています。
今後につきましては、ディスクロージャーの透明性を高めるため一層説明責任を充実するとともに、さらなる経営のチェック機能強化を図ってまいります。
<実施しない主な原則とその理由>
当社は、JASDAQ上場企業としてコーポレートガバナンス・コードの基本原則をすべて実施しております。
基本的な考え方
当社は、技術革新と創造性を発揮し、質の高い優れた製品とサービスの提供を通じ人々の健康と福祉に貢献していくことを使命とし、全ての企業活動において品質を高めるべく企業統治の整備を進めています。
今後につきましては、ディスクロージャーの透明性を高めるため一層説明責任を充実するとともに、さらなる経営のチェック機能強化を図ってまいります。
<実施しない主な原則とその理由>
当社は、JASDAQ上場企業としてコーポレートガバナンス・コードの基本原則をすべて実施しております。
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2025 Investment Bridge Co.,Ltd. All Rights Reserved. |





