ブリッジレポート:(7776)セルシード vol.6
| (7776:JASDAQ) セルシード |
|
||||||||
|
||||||||
企業名 |
株式会社セルシード |
||
社長 |
長谷川 幸雄 |
||
所在地 |
東京都新宿区若松町33-8 アール・ビル新宿 |
||
決算期 |
12月末日 |
業種 |
精密機器(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2010年12月 | 66 | -1,204 | -1,002 | -1,009 |
| 2009年12月 | 87 | -785 | -788 | -790 |
| 2008年12月 | 61 | -778 | -644 | -650 |
| 2007年12月 | 40 | -809 | -614 | -616 |
| 2006年12月 | 23 | -672 | -464 | -470 |
| 2005年12月 | 34 | -412 | -336 | -343 |
| 2004年12月 | 53 | -257 | -214 | -215 |
| 株式情報(11/22現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
細胞シート再生医療事業
細胞シート再生医療医薬品(各種用途の「細胞シート」)及びその応用製品を販売する。現在、共同研究先と5つの再生医療製品パイプライン(新薬候補)の研究開発を進めている。
再生医療支援事業
細胞シート再生医療の基盤ツールである温度応答性細胞培養器材及びその応用製品を開発・製造(多額の設備投資を必要とする一部の工程は外部委託)し、世界各国の大学・研究機関等に提供している。当事業は細胞シート再生医療事業の提携先開拓のための戦略的な意義をも有し、収益だけを目的とした事業ではない。
 |
| 2011年12月期第3四半期決算 |
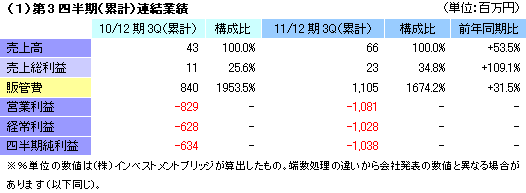 損失拡大ながら想定の範囲内
細胞シート再生医療事業の売上計上は無かったが、再生医療支援事業にかかる売上66百万円を計上した。再生医療支援事業では、昨夏に投入した新規商材 細胞タイトジャンクションリアルモニタリングシステム「cellZscope」の販売が好調で、通期の売上目標(68百万円)に対する進捗率は97%に達した。損益の面では、研究開発費(392百万円→678百万円)を中心にした販管費の増加で営業損失が拡大したものの、想定の範囲内。営業外損益が悪化したのは、補助金収入が減少したため(226百万円→55百万円)。尚、細胞シート再生医療事業では、9月の第65回厚生労働省厚生科学審議会科学技術部会において、共同研究先による「軟骨再生シート」に関する臨床研究実施計画を了承する方向性が示された。今後、臨床研究の開始が認められる見通しで、これにより細胞シート再生医療医薬品パイプライン5つ全てが臨床研究又はそれ以降の段階に入る事となった。  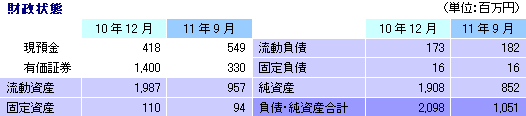 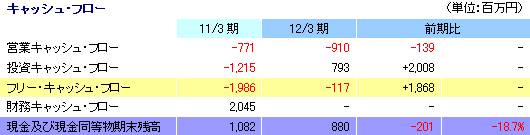  (3)第3四半期(7-9月)のトピックス
第3四半期には、細胞シート再生医療関連の特許や細胞シート工学応用特許が成立した他、欧州における事業推進体制の強化や新株予約権を活用した資金調達枠の設定等、今後の事業展開に向けた事業体制や財務面での施策も進んだ。
①細胞シート再生医療関連特許の成立
8月に細胞シート再生医療関連(表皮培養シート、重層化培養皮膚シート及びそれらの製造法)の特許が海外で成立した。特許の登録国は、フランス、イギリス、ドイツ、イタリア、オランダ、スペイン、スウェーデン、ベルギー、ギリシャ、フィンランドの10か国(日本では4月に成立)。今回成立した特許は、細胞シート工学に基づいて表皮細胞シートや重層化した皮膚シートを作製する技術の基本コンセプトを示すもので、角膜再生上皮シートや食道再生上皮シート等の表皮系・粘膜系組織の再生に広く応用できる可能性を示している。また、9月には移植用「歯周組織再生シート」に関する特許が日本で成立した。この特許は細胞シート再生医療医薬品パイプラインの1つである歯周組織再生シートの作製技術に関する特許であり、既存の治療法では困難であった歯周病の根本的な治療(歯根膜組織の再生、中等度段階での治療を通じた歯の喪失の防止等)及び既存法よりも短い期間での治癒につながる可能性を示している。いずれの特許も、細胞シート再生医療の新規性・進歩性を示唆するものであると考える事ができる。
②細胞シート工学応用特許の成立
細胞シートを利用した癌組織モデル作製技術に関する特許が、8月に日本で成立した。この特許は、細胞シート工学の応用展開に関する特許で、細胞シート工学を用いて医薬品候補物のスクリーニング等に用いられる評価実験用動物を作製する際に必要な特許となる。今回の特許成立は、細胞シート工学が、再生医療プラットフォーム技術としてのみならず、医薬品研究開発支援や製品開発支援の面でもイノベーションをもたらす可能性がある技術である事を示している(例えば、新しい抗癌剤の研究開発において、必要な期間・投資額・実験動物数等の削減やその開発成功確率の向上に寄与する)。
③欧州における事業体制の強化
直近までの事業進捗状況を踏まえ、欧州における事業体制を強化するべく、欧州地域総責任者を任命した他、欧州角膜再生上皮シート販売及びマーケティング体制の強化に着手した。
・同社グループ欧州地域総責任者の任命
同社グループの欧州地域総責任者にHelmut Hasibeder 氏を任命した。同氏は、オーストリア・ウィーン大学医学部を卒業し臨床の現場経験も持つ医師だが、社長として武田薬品グループのオーストリア法人を立ち上げ、同社を欧州武田薬品グループトップの市場シェア(当時)を有する企業に育て上げた実績を持つ他、世界的バイオ医薬品企業である米Amgen Inc.等での勤務経験も有する。今後、欧州地域総責任者として同社グループの欧州地域での事業活動を現地で統括する(特に喫緊の課題である角膜再生上皮シートの事業化準備を中心とした具体的な実務の推進役となる)。
・欧州角膜再生上皮シートの販売及びマーケティング体制の更なる強化
6月の欧州薬事申請提出及び上述のHasibeder氏の加入等を踏まえて、改めて欧州販売・マーケティング体制に関する戦略的自由度の見直しに着手した。その第1弾として実施したのが、Clonmel Healthcare Limited 社との販売提携解消であり、今後、提携網の拡充、自販組織の構築、提携と自販の組み合わせの3つの可能性を視野に入れ欧州事業の準備を進めていく考え。
④新株予約権を活用した資金調達枠の設定
角膜再生上皮シートにおける欧州での事業化と米国展開を見据えて財務基盤を強化するべく、新株予約権を活用した総額約1,000百万円の資金調達枠を設定した。新株予約権は、4回号から8回号までの5回号に分けられ、1回号あたりの新株予約権は4個で額面200百万円(額面200百万円×5回号=1,000百万円)。
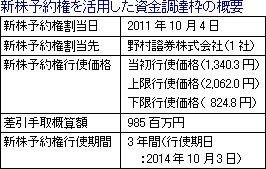 ※ 新株予約権の行使を促進し早期に資金調達を実現するべく、10月25日に新株予約権行使価格の修正を行った。
4億円分(第4回及び第5回新株予約権)を対象に、11月11日までの行使価額を824.8円とした(22日以降の行使価格については、1,340.3円に修正)。11月21日時点で、100百万円が行使済み。 |
| 2011年12月期業績予想 |
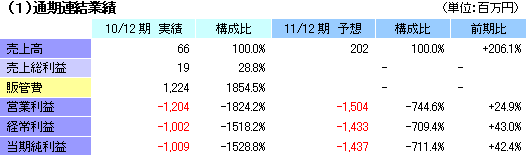 通期業績予想に変更は無く、1433百万円の経常損失見込み(同1002百万円の損失)
売上高は前期206.1%増の202百万円。内訳は、再生医療支援事業が68百万円、細胞シート再生医療事業が134百万円。細胞シート再生医療事業では、角膜再生上皮シートの米国展開に伴う個別契約の一時金収入127百万円(期初予想107百万円)及び人道的使用制度に基づく製品提供にかかる売上7百万円を見込んでいる。利益面でも、上記の細胞シート再生医療事業の売上の上振れ分が上乗せされ、期初予想を上回る見込み。
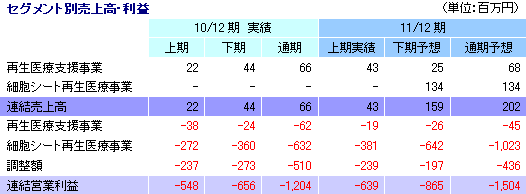  |
| 細胞シート再生医療と「iPS細胞」との関係について |
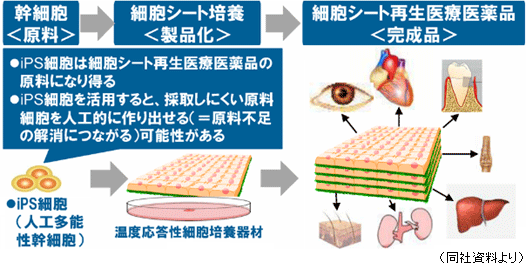 |
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2026 Investment Bridge Co.,Ltd. All Rights Reserved. |




