ブリッジレポート:(2183)リニカル vol.15
| (2183:東証1部) リニカル |
|
||||||||
|
||||||||
企業名 |
株式会社リニカル |
||
社長 |
秦野 和浩 |
||
所在地 |
大阪市淀川区宮原1-6-1 新大阪ブリックビル |
||
決算期 |
3月 |
業種 |
サービス業 |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2012年3月 | 3,110 | 728 | 723 | 424 |
| 2011年3月 | 2,512 | 288 | 278 | 147 |
| 2010年3月 | 2,404 | 480 | 473 | 273 |
| 2009年3月 | 2,036 | 549 | 515 | 300 |
| 2008年3月 | 1,273 | 505 | 494 | 296 |
| 2007年3月 | 613 | 186 | 195 | 114 |
| 2006年3月 | 118 | 16 | 19 | 11 |
| 株式情報(6/10現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
CRO事業では、治験の最も大切な段階である第II相試験(フェーズII)及び第III相試験(フェーズIII)における「モニタリング業務」に特化している事が特徴。また、統合失調症、うつ病、アルツハイマー等の中枢神経系(Central Nervous System :CNS)領域やがん領域といった難易度の高い領域に注力する事で他社との差別化を図っている(これに対して、生活習慣病等の領域は差別化が難しく受託競争が激しい)。一方、CSO事業では、定の疾患領域にフォーカスすると共にCRO事業で培ったノウハウを活かし、プロダクトマーケティング業務や市販後データの企画・収集業務の受託を手掛けており、MR派遣が中心の他社のCSO事業と一線を画している。 主な取引先は、武田薬品工業グループ、第一三共、エーザイ、大塚製薬、塩野義製薬等の国内主要製薬会社。尚、第II相試験は安全性及び有効性・用法・用量を調べるために実施され、この結果を基に第III相試において、実際の治療に近い形での効果と安全性を確認する。 【沿革】
2005年6月、藤沢薬品工業株式会社(現 アステラス製薬株式会社)で免疫抑制剤等の開発に携わってきたメンバー9名によって設立された。大阪発理想の医薬品開発受託(CRO)事業を目的として、設立当初から、CNS領域やがん領域の育成に取り組み、会社設立後まもなく大塚製薬からCNS領域の案件を受注。その後、人材を補強し事業部として受注活動を強化した。また、がん領域も外資系製薬会社等でがん領域の医薬品開発を手掛けた人材等に恵まれ、足元、受注が拡大している。SMO(治験施設支援機関)事業進出を念頭に、06年1月に同事業を手掛けるアウローラ(株)を子会社化したが、CRO事業への経営資源集中を図るべく07年5月に全保有株式を売却。08年7月に、国内の製薬会社の米国進出支援を目的に米国カリフォルニア州に全額出資子会社LINICAL USA, INC.を設立。同年10月の東証マザーズ上場を経て、13年3月に東証1部に市場変更となった。 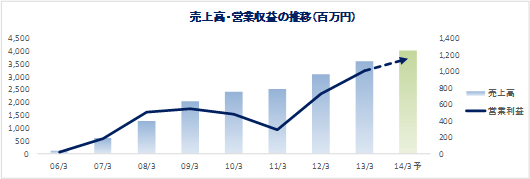 【業務内容】
事業セグメントは、主力のCRO事業とCSO事業に分かれ、13/3期の売上構成比は、それぞれ95.3%、4.7%。CRO事業は「モニタリング業務」に特化しており、これに付随する「品質管理業務」や「コンサルティング業務」も手掛ける。一方、CSO事業は、プロダクトマーケティング業務や市販後データの企画・収集業務の受託を手掛け、MR派遣を中心とする他社と差別化を図っている。
  【強み】
(1)難易度が高く競争相手が少ないがん領域や中枢神経系領域のモニタリング業務に強み
難易度が高く競争相手が少ないがん領域や中枢神経系領域のモニタリング業務に強みを有する。例えば、がん領域であれば、薬の副作用によるものか、がんの進行によるものか、安全性評価が難しく、中枢神経系領域であれば、例えばアルツハイマー病の患者は問診等による薬の有効性評価が難しいため、モニタリングでは高度な対応が必用とされる。この他、急性疾患や特定疾患(いわゆる難病)と呼ばれる領域も難易度が高い分野で、がん領域や中枢神経系領域と共に新薬開発が活発だ(しかし、対応できるCROは限られる)。一方、生活習慣病の治験は患者の状態が比較的安定しており、有効性評価についても比較的容易であるため、難易度は低い(例えば、糖尿病では血糖値の測定データの収集が中心)。 新薬の開発トレンドは生活習慣病から治療満足度が低いがん領域や中枢神経系領域にシフトしているが、上記の通り、がん領域では安全性情報の取り扱いが難しく、中枢神経系領域では有効性評価の標準化が難しい。このため、これまでは製薬会社が社内で対応していたが、近年、こうした難易度の高い領域でもアウトソーシングされるケースが増えている。同社にとって、中枢神経系領域は会社設立時からの注力分野であり、がん領域は2年前にアストラゼネカのイレッサ開発メンバーを迎え受注活動を本格化した。13/3期末受注残高47億50百万円に対して、がん領域は11億55百万円(構成比24%)、中枢神経領域は19億98百万円(同42%)。 (2)高い収益性
有効性確認や安全性確認といった臨床の現場での高い業務遂行力に加え、CRO業務全般での知識・技術水準の高さも同社の強みである。同社が手掛ける案件の逸脱率は非常に低く抑えられており、また、症例の組み入れやデータの回収期間を含め、全案件の8割程度は実施期間の短縮に成功している。同社は難易度の高い分野で高品質・短納期を実現しているため適正価格での受注が可能であり、スケールメリットのハンデを補って大手を凌ぐ利益率を実現している。尚、収益力の源泉となるのがCRAの質だが、同社CRAの質の高さを示す一例として、GCPパスポート認定試験の合格率をあげる事ができる。GCPパスポート認定試験とは、国際共同治験に対応できる人材の育成を目的にした試験で、日本臨床試験研究会が実施している。 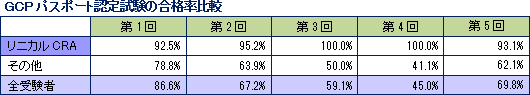  |
| 経営戦略 |
|
(1)CRO事業
CRO事業は第II相試験、第III相試験における「モニタリング業務」に特化し、また、がん領域や中枢神経系領域といった難易度の高い領域で評価を得ている。引き続き高難易度領域で実績の積み上げを図ると共に、事業の拡大に向けCRAを増員していく(早期270名体制の確立)。
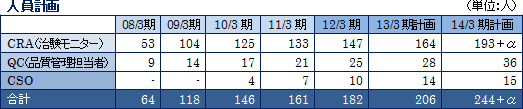 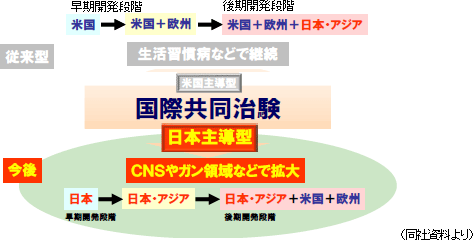  (2)CSO事業
他社が手掛けるMRの派遣サービスとは一線を画し、同社が主体となって業務を進める請負サービス型のCSO事業を志向している。具体的には、特定の疾患領域やエリアで経験豊富なMRを採用し、CRO事業部で蓄積したノウハウを活用する事で専門性の高い業務を受託し差別化を図っていく考えで、現在、プロダクトマーケティング業務と市販後データの企画・収集業務の受託が2本柱。今後は、これら2事業の強化に加え、市場拡大が期待できる臨床研究のグローバル案件等の受託事業を第3の事業として育成していく。尚、13/3期は医師主導臨床研究の受託に成功し、セグメント損益が黒字転換する原動力となった。  CRO事業とCSO事業により開発から販売後までをカバーする
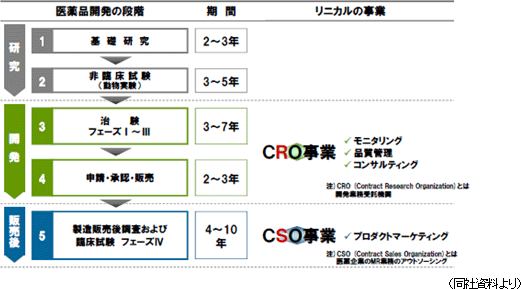 (3)創薬支援事業(新規事業の育成) 短期業績に影響の少ない新薬開発スキーム、アジア諸国のドラックラグ化合物の積極的な開発、更には開発計画作成から申請までのワンストップ委託といった昨今のニーズへの対応を念頭に創薬支援事業を育成していく。このため、治験実施計画書作成、データ回収以降の業務を含む案件の戦略的な受託と経験の蓄積に取組んでいく考えである。
|
| 2013年3月期決算 |
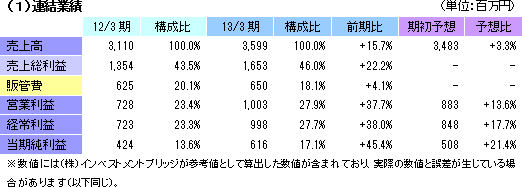 営業利益が過去最高を更新
売上高は前年同期比15.7%増の35億99百万円。CRO事業は、上期に中止案件が発生したものの、既存プロジェクトの増員及び新規案件の獲得による受注増で吸収。医師主導臨床研究の受託でCSO事業の売上も増加した。
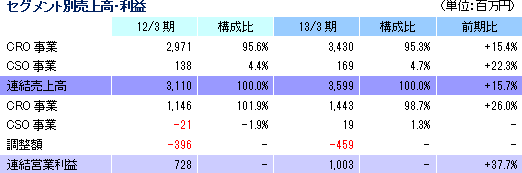 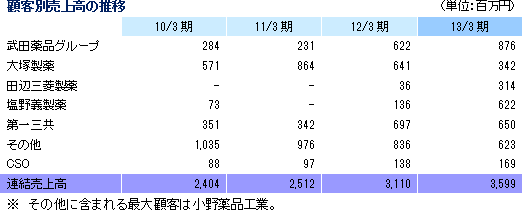 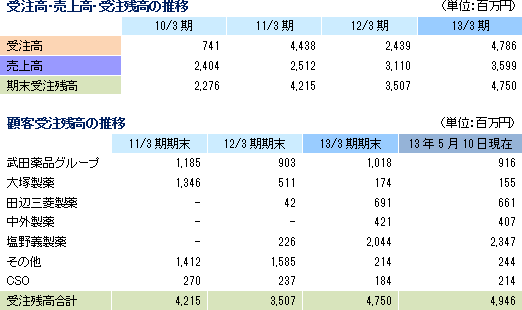 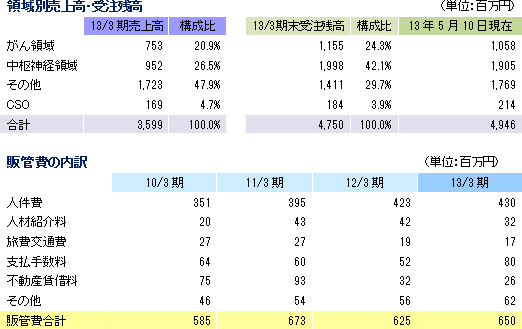 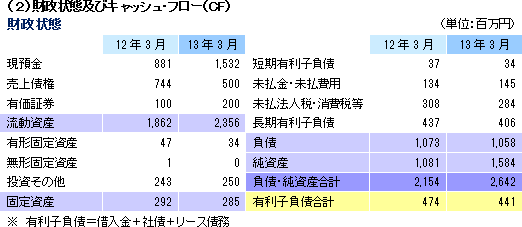  |
| 2014年3月期業績予想 |
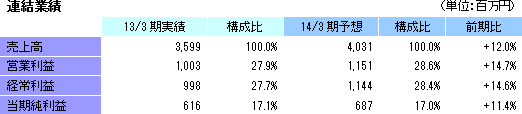 前期比12.0%の増収、同14.6%の経常増益予想。8期連続増収、3期連続過去最高益更新を見込む
売上高は前期比12.0%増の40億31百万円。一部受託内定案件の期ズレを想定するなど慎重な予想となったものの、既存プロジェクトの増員と新規案件の受注で吸収し8期連続の増収を見込んでいる。利益面では、CRAの増員やグローバル展開に伴い営業費用が増加するものの、増収効果で吸収し営業利益は11億51百万円と同14.7%増加。3期連続の最高益更新が見込まれる。配当は記念配を落とし1株当たり14円の期末配当を予定している。 |
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2026 Investment Bridge Co.,Ltd. All Rights Reserved. |




