ブリッジレポート:(4583)カイオム・バイオサイエンス 2025年12月期決算
 小池 正道 社長 | 株式会社カイオム・バイオサイエンス(4583) |
 |
企業情報
市場 | 東証グロース市場 |
業種 | 医薬品(製造業) |
代表取締役社長 | 小池 正道 |
所在地 | 東京都渋谷区本町3-12-1 住友不動産西新宿ビル6号館 |
決算月 | 12月末 |
HP |
株式情報
株価 | 発行済株式数 | 時価総額 | ROE(実) | 売買単位 | |
107円 | 68,453,800株 | 7,324百万円 | -65.1% | 100株 | |
DPS(予) | 配当利回り(予) | EPS(予) | PER(予) | BPS(実) | PBR(実) |
0.00 | - | - | - | 16.18円 | 6.6倍 |
*株価は3/13終値。25年12月期決算短信より。創薬事業における合理的な業績予想の算定が困難なため、26年12月期の業績予想について会社側は創薬支援事業の売上高600百万円のみ開示している。
業績推移
決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 | EPS | DPS |
2021年12月 | 712 | -1.334 | -1.329 | -1.479 | -36.74 | 0.00 |
2022年12月 | 630 | -1,258 | -1,243 | -1,242 | -28.26 | 0.00 |
2023年12月 | 682 | -1,205 | -1,217 | -1,220 | -24.62 | 0.00 |
2024年12月 | 780 | -1,030 | -1,019 | -1,020 | -17.54 | 0.00 |
2025年12月 | 593 | -979 | -989 | -982 | -14.47 | 0.00 |
2026年12月(予) | - | - | - | - | - | 0.00 |
*単位:百万円、円。創薬事業における合理的な業績予想の算定が困難なため、26年12月期の業績予想について会社側は創薬支援事業の売上高600百万円のみ開示している。
株式会社カイオム・バイオサイエンスの2025年12月期決算概要、事業の進捗などをお伝えします。
目次
今回のポイント
1.会社概要
2.2025年12月期決算概要
3.2026年12月期の見通し
4.今後の注目点
<参考:コーポレートガバナンスについて>
今回のポイント
- 「バイオシミラー医薬品事業」に関し、バイオシミラー医薬品の原薬・製剤製造を行う合弁会社の設立が決定したほか、カイオム・バイオサイエンス、アルフレッサ ホールディングス、キッズウェルの3社でバイオシミラー医薬品開発に関する基本合意書と個別製品の共同開発のための基本契約書を締結した。製造施設の整備完了後、新規バイオシミラー医薬品の製造を移管することを想定しており、現在の委託先であるMBIと連携することで、スムーズな技術移管と稼働、バイオシミラー医薬品の安定供給体制構築を実現する。新規開発から製造・供給までをカバーする国内初のバイオシミラー医薬品のサプライチェーン構築と安定供給の実現にむけた取り組みをさらに推進する考えだ。
- 2025年12月期の売上高は前期比24.0%減(1億87百万円減)の5億93百万円。創薬支援事業は増収。アルフレッサ ホールディングス株式会社(東証プライム、2784)とのバイオシミラー医薬品の共同開発契約締結に伴う収益を計上した。抗体創薬の技術・サービスは高い評価を得ており、既存顧客との取引は安定的に推移。日東紡績株式会社等、複数の新規顧客獲得も進んだ。営業損失は同51百万円縮小の9億79百万円。研究開発費が同1億60百万円減少した。主に高額設備費等の減少によるものである。
- 2026年12月期の業績予想については、創薬事業における合理的な業績予想の算定が困難なため、創薬支援事業の売上高6億円のみ開示している。創薬事業においては、CBA-1205及びCBA-1535の第1相試験の終了に向けた着実な進展を目指すとともに、これら臨床2品目や非臨床段階のパイプラインを含めた導出候補品の導出活動、二重特異性抗体作製技術や創薬ノウハウを用いた製薬会社とのコラボレーションを推進する。創薬支援事業は、技術サービス力を活用し既存顧客ニーズに対して丁寧に対応するとともに、業務提携契約にもとづく拡販体制を活用するなどして、安定的な収益基盤として抗体作製やタンパク質調製等の受託業務を推進する。IDDビジネスやバイオシミラービジネスにおける新薬開発やバイオシミラー開発から獲得する収益の拡大を企図した活動も並行して取り組んでいく。
- バイオシミラー医薬品開発に伴う収益を計上したことも寄与し、減収を見込んでいた創薬支援事業は小幅ではあるが増収となった。新規顧客開拓も進んでいるようで、収益基盤強化が進んでいる。リスク・リターンの面からは、創薬支援事業と創薬事業の中間に位置し、2025年以降の事業展開における収益力の強化とそれによる経営基盤の安定化に資するものと位置付けるIDDビジネスも、バイオシミラー医薬品事業とともに着実に進捗を示している。中心的な開発品である「CBA-1205」「CBA-1535」におけるライセンス契約の獲得動向とともに、引き続き各事業の進捗に注目していきたい。
1.会社概要
ミッションに「医療のアンメットニーズ(※)に創薬の光を」を掲げ、独自技術であるADLib®システム等の複数の抗体作製技術を駆使して最適な抗体を取得し、アンメットニーズの高い疾患に対する抗体医薬品の開発候補品創出に取り組むバイオベンチャー。高い抗体開発候補品創出能力などが強み。
※アンメットニーズ
現状では有効な治療法がなかったり、薬剤による治療満足度が低かったりする治療に対する未充足なニーズ
【1-1 沿革】
2005年2月、国立研究開発法人理化学研究所の太田邦史研究員(現:東京大学執行役・副学長)が率いる遺伝ダイナミクス研究ユニットと財団法人埼玉県中小企業振興公社(現:財団法人埼玉県産業振興公社)との共同研究により開発された抗体作製基盤技術ADLib®システム(アドリブシステム)の実用化を目的として設立された。
設立当初よりADLib®システムの技術導出(ライセンス供与)を中心的なビジネスモデルと位置付けて活動してきたが、2017年にADLib®システムの技術導出に依存したビジネスモデルから、創薬開発を推進する経営へと軸足をシフトさせ、経営ビジョン、経営方針、ビジネスモデルの変更も行った。
2020年には自社開発品の初期臨床試験を開始し、臨床開発ステージのバイオベンチャーとして成果創出に取り組んでいる。
2011年12月に東証マザーズに上場。2022年4月、市場再編に伴い、東証グロース市場に移行。
【1-2 経営理念など】
Mission | 医療のアンメットニーズに創薬の光を |
Vison | アンメットニーズに対する抗体医薬の開発候補品を生み出すNo.1ベンチャー企業を目指す |
経営方針 | ●健全な経営と信頼性の確保を第一に、社会とともに成長する企業を目指す。 ●創造と科学をもってアンメットニーズに対する治療薬を開発して、患者さんと社会へ貢献する。 ●外部連携により継続的なパイプライン創出と企業価値向上を実現する。 |
後述するように、同社の主力製品である抗体医薬はがんや自己免疫疾患の領域では目覚ましい治療効果をもたらしている。しかし、膵臓がん、肺がん、アルツハイマー病、糖尿病合併症、筋萎縮性側索硬化症(ALS)等、未だに治療満足度、薬剤貢献度が低い疾患が残されているほか、既存の抗体治療薬よりも優れた抗体に対するニーズも存在する。
同社は、この経営理念の下、抗体作製・タンパク質調製関連技術で構成される自社技術プラットフォームを最大限に活用して、アンメットニーズの高い分野に対する抗体創薬に取り組んでいる。
【1-3 市場環境】
◎抗原抗体反応と抗体医薬品
同社の事業内容を理解するうえで知っておく必要のあるキーワードが「抗原抗体反応」、「抗体医薬品」などである。
ヒトには、体内に侵入した細菌やウイルス等のタンパク質を異物(抗原)として認識し、その異物を攻撃、排除するために、体内で抗体を作って身体を守る防御システムが備わっており、これを「抗原抗体反応」と呼ぶ。
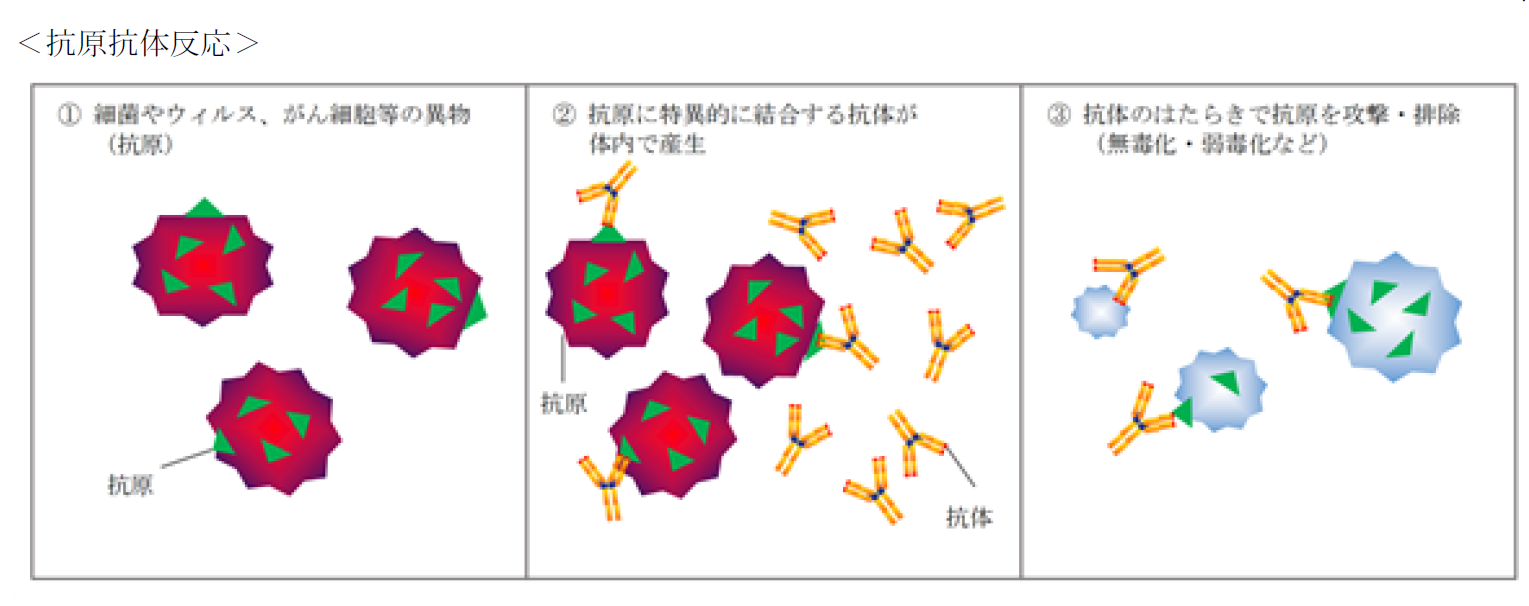
(同社有価証券報告書より)
こうして産生された抗体は、特定の抗原にのみ結合する性質を持っており、正常な細胞とがん細胞を見分けたり、病気の原因となるタンパク質の機能を抑えたりすることができる。
この抗体の特徴を医薬品に活用したものが「抗体医薬品」である。
従来の抗がん剤等の中には、正常な細胞にも作用して副作用を引き起こすものも多く、副作用を抑制するために本来の目的であるがん治療を進めることができないといったケースも見られるが、抗体医薬品は、疾患に関連する細胞に特異的に発現が認められる抗原をピンポイントで狙い打ちするため、高い治療効果と安全性が見込まれ、近年市場が拡大している医薬品である。現在、世界で承認されている抗体医薬は100品目を超えており、がんや自己免疫疾患の領域で目覚ましい治療効果をもたらしたものもある。
(抗体医薬品が使われている主な疾患)
分類 | 病気 |
がん | 大腸がん、乳がん、非小細胞肺がん、メラノーマ、腎がん、前立腺がん、胃がん、急性骨髄性白血病、非ホジキンリンパ腫、皮膚T細胞リンパ腫等 |
アレルギー・免疫 | 関節リウマチ、多発性硬化症、クローン病、喘息、腎臓移植後の急性拒絶(正)反応 |
その他 | 黄斑変性症、骨粗鬆症、感染症 |
◎成長が続くバイオ医薬品市場
バイオ医薬品は、遺伝子組換え技術等のバイオテクノロジーにより創出された医薬品であり、1980年代から実用化が始まった。その後、抗体作製技術等の技術革新により、分子量が大きく、構造が複雑な抗体医薬品の創出が可能となり、新たな治療手段として、前記のような有用性の高さが臨床的に示されている。
バイオ医薬品の牽引役である抗体医薬においては、京都大学高等研究員の本庶佑特別教授がノーベル医学生理学賞を受賞したことで話題になったオプジーボなどに代表される免疫チェックポイント阻害剤(※)が複数製品化され、順次市場は拡大されている。近年の全世界医療用医薬品市場においては、抗体薬品を中心とするバイオ医薬品処方箋薬のシェアは4割を超え、売上高の上位100品目の半数以上を占めるまでになっている。
加えて、他の抗体医薬品との併用療法によるがん治療の向上を目指した開発研究が多数実施されているほか、抗体薬物複合体(ADC)やバイスペシフィック抗体(※)に代表される多価抗体などの次世代型抗体については、従来よりも有用性を高めた医薬品として上市されている。
高い薬効および安全性というアドバンテージから、世界の医薬品売上高上位には抗体医薬品製剤が多数ランクインしており、今後も免疫チェックポイント阻害剤を含めた抗体医薬品市場は一層の拡大が期待されている。
※オプジーボ
一般名はニボルマブ。がん細胞が免疫システムを無効化する仕組みを阻止する働きを持つ免疫チェックポイント阻害剤の一つ。日本では、2014年7月に切除術による根治が期待できない悪性黒色腫の治療薬として承認され、同年9月から小野薬品工業が販売を開始した。その後、15年12月に非小細胞肺がん、16年9月に腎細胞がんにも適応が拡大された。
※免疫チェックポイント阻害剤
免疫療法の一種。これまでの免疫療法は免疫細胞の攻撃力を高める「アクセルを踏む働き」が中心であったのに対し、がん細胞によって免疫細胞にかけられたブレーキ(免疫チェックポイント)を外すことにより、免疫細胞の本来の力を発揮させ、がん細胞を攻撃できるように作用するもの。従来の治療法では効果が十分に見られなかった患者にも治療効果を上げることに成功している。
※バイスペシフィック抗体
通常、抗体は抗原を認識する部位を2つ持っており、それらは同じ抗原を認識する。それに対し、2つの抗原認識部位がそれぞれ別のターゲット(抗原)を認識するものをバイスペシフィック抗体と呼ぶ。
【1-4 事業内容】
報告セグメントは、独自の抗体作製技術ADLib®システム、Tribody®、DoppeLib™等の抗体作製技術を用いて治療薬等の抗体医薬品候補を開発し、これを導出する「創薬事業」および、抗体作製技術を用いて製薬企業や診断薬企業、大学等の研究機関で実施される創薬研究を支援する「創薬支援事業」の2つ。
◎抗体作製技術について
抗体医薬品を創り出すために不可欠な抗体作製技術には様々な種類が存在する。
同社独自技術であるADLib®システムは、従来の抗体作製技術とは異なるテクノロジーで「従来の免疫法では困難な抗原に対する抗体取得が可能」、「迅速な抗体取得」などの技術的特徴を有している。ADLib®システムに加え、次世代抗体として研究開発が行われている多価抗体作製技術のTribody®、二重特異性抗体ハイスループット作製技術のDoppeLib™を保有している。ハイブリドーマ法などのコンベンショナルな技術を含めてそれぞれの技術の特性を活かして統合的に運用することにより抗体作製力の強化を進めている。
<抗体作製技術とその特徴>
抗体作製技術 | 特性 |
ADLib®システム | ●抗原があれば10日前後と短期間でヒトIgG抗体を獲ることができる。 ●自律的多様化という独創的な抗体ライブラリの特徴を生かし、抗原特異的抗体の取得から抗体の高親和性化までを連続的に行うことが可能。 ●動物免疫と異なり、自己抗原への免疫寛容の影響を受けないため、理論的にはあらゆる配列のタンパク質を認識する抗体が取得できる可能性がある。 |
Tribody® (多重特異性抗体作製技術) | ●3つ以上の異なる抗原結合部位を持つ抗体であるTribody®およびその発展型多重特異性抗体のデザイン・エンジニアリング・創薬開発を可能にする技術プラットフォームをいう。 ●CBA-1535のように腫瘍細胞の近傍でT細胞を活性化することにより、がん細胞を叩くT cell engagerというカテゴリや、複数の疾患関連細胞を架橋することでがん以外の疾患の治療薬も設計可能。 |
ハイブリドーマ法 | ●動物免疫による抗体作製法で、最もよく用いられる。 ●手法が確立されており、医薬品化された実績も多い。 ●ヒト抗体産生動物を用いた場合、ヒト化の工程を経ずにヒト抗体を取得することができる。 |
DoppeLibTM | ●二重特異性抗体作製のハイスループットを実現できる先進的な技術を構築中。研究サイクルの高速化に繋がると期待している。 ●複数の企業とコラボレーション中である。 |
(1)創薬事業
アンメットニーズの高い疾患領域における抗体創薬の自社開発または共同開発を行い、その成果物である抗体に関する特許権等の知財権を製薬企業等に実施許諾し、契約一時金、マイルストーン、およびロイヤルティ等の収入を獲得していく事業で、同社の成長を担っている。
◎事業範囲
医薬品の研究開発プロセスのうち、「抗体の作製・評価」「開発・製造」「臨床試験の一部」を事業範囲としている。
タンパク質調整、抗体作製、創薬研究、臨床開発の研究開発機能を有し、新規抗体創製から初期臨床開発を実施できる研究開発体制を構築している。
◎創薬事業のビジネスモデル
様々な抗体作製技術を駆使して、アンメットニーズの高い疾患領域における抗体創薬開発を行い、前臨床開発または初期臨床開発段階で開発した医薬候補品を製薬企業等に導出。契約一時金、マイルストーン収入(開発&販売)、およびロイヤルティ収入等を獲得する。抗原や研究用抗体の取得についてはアカデミア(大学・研究機関)に対する積極的なアプローチにより連携を強化、有望なシーズについての事業化権を獲得する。
複数の医薬品候補を導出することにより、投資フェーズから収益フェーズへの転換を図る。
◎開発の基本戦略・方針
特にがん領域においては自社で開発候補抗体(ヒト化抗体、ヒト抗体)の非臨床データパッケージまで作製できる研究体制を構築し、前臨床段階での導出を基本戦略としているが、初期臨床試験まで自社で対応できる開発体制の構築し、2020年には自社パイプラインの臨床開発を開始した。
これは、同社が導出したいタイミングで必ずしも適切な導出先が見つかるかは明確ではないこと、ある程度開発を進めて付加価値を付けた後に導出したほうが事業として明らかに良好な場合もあることを想定しているためである。
また、今後の展開については、開発遅延・中止リスクを鑑み、継続的に10程度の探索ステージのプロジェクトを運営し、創薬成功確率を高めることを方針として掲げている。
◎主要パイプラインおよび開発状況
(自社開発品)
CBA-1205(ADCC活性増強型ヒト化抗DLK-1モノクローナル抗体) | |
概要 | 「DLK-1」をターゲットとするファーストインクラスのヒト化モノクローナル抗体。DLK-1は幹細胞や前駆細胞のような未熟な細胞の増殖・分化を制御し、これまでに肝臓がんをはじめとする複数のがん細胞表面においても発現し、その増殖に関与していることが明らかとなった新しいがん治療の標的になる可能性がある分子。 |
想定適応疾患と解決すべきアンメットニーズ | 難治性の癌腫である肝細胞がん、肺がん等。 肝細胞がん、メラノーマを始めとした有効な治療薬がない悪性度の高い腫瘍に対する新たな治療薬を提供する。さらに小児がんを対象とした臨床試験も行われている。 |
知財 | 日本・米国・欧州・中国他で特許成立。 |
開発の進捗 | 2020年7月にスタートした国内臨床試験第1相試験では、固形がん・肝細胞がん患者を対象に、安全性・忍容性・体内動態および有効性評価を実施する。
2022年に終了した同試験の前半パートでは、固形がん患者を対象とした治験経過から標的および本抗体の安全性の高さが示された。前半パートで登録されたメラノーマ(悪性度の高い皮膚がんの一種)の患者で腫瘍縮小を伴うSD(安定)評価が続き、48ヶ月を超える長期継続投与を確認し、現在も投与継続中である。
2022年に開始された後半パートでは、前半パートでの最大量を参考に、肝細胞がん患者の臨床試験における最適な投与量を確認するほか、安全性と初期の薬効シグナルを評価している。この薬効シグナルの確認が早期導出の鍵となる。後半パートで登録された肝細胞がん患者1例においてPR(部分奏功:30%以上の腫瘍縮小)を確認した。 前半パートにおける長期投与実績に基づき2024年よりメラノーマパートを推進している。 スペインのGermans Trias i Pujol Research Instituteと本剤に関連する共同研究を進めてきたが、その共同研究において小児がんへの適応可能性を示唆する研究成果が確認されたため、2025年に神経芽腫や肝芽腫をはじめとする小児がんパートを追加することを決定し、症例登録を開始した。 |
導出活動 | 肝細胞がん、メラノーマ、小児の固形がんを対象に、製品価値最大化と導出時の経済条件向上を目指し、事業提携や導出活動を継続している。 |
CBA-1535(ヒト化抗5T4・抗CD3多重特性抗体) | |
概要 | 3つの分子を認識するTribody®技術を用いて創製したがん治療用抗体。 臨床標的としての安全性が確認されている既知(公知)のがん抗原5T4と免疫細胞であるT細胞 上のタンパク質CD3を標的とする多重特異性抗体。 |
想定適応疾患と解決すべきアンメットニーズ | 悪性中皮腫、小細胞肺がん、非小細胞肺がん等。 T細胞の増殖と活性化を誘導して強力な細胞傷害活性を発揮する(T Cell engager)。Tribody®としては初めての臨床開発品目であり、薬剤治療の選択肢が少なく、予後の悪い悪性中皮腫を始めとした固形がんに対する有効な治療薬を提供する。 |
知財 | 日本・米国・英国・欧州・中国等で成立。 |
開発の進捗 | 2022年6月、Tribody®抗体として世界初の臨床試験(臨床第1相試験)が始まり、第一例目の被験者への投与が開始された。 前半パートでは、固形がん患者を対象に単剤を投与。低用量から段階的に投与し、安全に投与できる最大量を求め、初期の薬効シグナルを評価中である。現時点では軽微な副作用のみ確認され、開発上の懸念を示すような安全性を懸念するデータは現れていない。本剤のコンセプトであるT細胞の活性化を示す血中バイオマーカーの変化が見え始めている。 こうしたことから、単剤パートのデータのみでの早期導出等の可能性も見据え、安全性および薬効シグナルの確認に向けて治験期間を延長することとした。プロトコルを改訂し、プレメディケーション(前投薬)を実施した上で投与用量の増量中である。
2026年中の開始を予定している後半パートでは、同じく固形がん患者を対象に、がん免疫療法薬との併用を行う。前半パートで安全性が確認できた用量から段階的に用量を上げながら、がん免疫療法薬と安全に併用できる最大量を求め、併用での初期の薬効シグナルを評価する。 |
導出活動 | 前半パートのデータ(単剤の安全性と有効性の評価)での導出を目指している。競争が激しくなりつつある固形がんのT cell engager領域において、開発資金力の高い企業への早期ライセンスによって本剤の開発の成功確度を向上させる考えだ。 |
(導出品)
PFKR(ヒト化抗CX3CR1抗体) | |
概要 | Fractalkine (CX3CL1) receptorの機能阻害抗体であり、自己免疫性神経疾患等の病態進行を抑制する治療用抗体 |
想定適応疾患 | 二次進行型多発性硬化症(SPMS)、神経変性疾患等 |
期待 | SPMSは難治性病型の多発性硬化症であり、安全性の高い有効な治療薬の開発が求められている疾患。 SPMSにおける病変(脱髄、神経変性)に直接的に関わると考えられる細胞傷害性のEomes陽性CD4+T細胞の機能を抑制することで症状の進行を抑制する事を期待。 |
知財 | 特許出願を完了 |
開発の進捗 | 国立精神・神経医療研究センターとの共同研究を進めた。 2024年11月、旭化成ファーマ株式会社との間で、独占的ライセンス契約を締結。旭化成ファーマに対して PFKR の全世界における独占的な開発、製造および販売権をサブライセンス権付きで許諾した。 契約一時金2億円を収受。以降は、将来的な開発及び販売の進捗に応じて最大約248億円のマイルストーンを受け取ることができるほか、製品上市後は、製品の売上高に応じたロイヤルティを受領する。 |
(導出候補品)
PCDC(ヒト化抗CDCP1抗体の薬物複合体) | |
概要 | ADC抗体を用いた新規パイプライン。標的分子はCDCP1ファーストインクラス抗体。 |
期待 | CDCP1は First in classとなる標的分子であり、標準治療耐性のがん種を含む幅広い固形がんで発現している。( 肺、結腸直腸、膵臓、乳、卵巣 がんなど)結合特性および毒性プロファイルに基づく、広い有効域&安全域が期待される。 |
知財 | 日本・中国で成立、米国・欧州他で出願中 |
進捗 | ADC用途を中心とした導出活動を推進中。国内外のカンファレンス等で導出候補企業へのコンタクトを進めているほか、ADC技術を保有する海外製薬企業との交渉を進めている。 カイオム・バイオサイエンスでは、「①独自のADC技術を持っているADC用の抗体が欲しい製薬企業」及び「②ADCとしてパイプラインを拡充したい製薬企業」を対象としてきたが、導出先企業のADC技術と同社抗体の組み合わせによる開発ニーズが高いことから、①の企業への導出活動を優先することとした。 |
PTRY(ヒト化抗5T4・抗CD3・抗PD-L1多重特性抗体) | |
概要 | 3つの分子を認識するTribody®技術を用いて創製したがん治療用抗体。 抗原結合部位の標的を①固形がんに発現が認められる 5T4②免疫細胞であるT細胞上のCD3③免疫チェックポイント阻害に関与するPD-L1、としたがん治療用抗体である。 この3つの組み合わせで、強い腫瘍増殖効果を発揮する。 |
想定適応疾患 | 悪性中皮腫、小細胞肺がん、非小細胞肺がん、トリプルネガティブ乳がん(TNBC)等 |
期待 | 従来のがん免疫療法では十分に効果が期待できなかった患者への新たな治療薬としての開発が期待されている。また、薬価抑制による医療経済への貢献にも有用と考えられている。 |
知財 | 特許出願を完了 |
進捗 | 非臨床試験中。イタリアの公的研究機関Ceinge-Biotecnologie Avanzateと行ったがん免疫療法に関する共同研究の成果が、国際的な学術雑誌であるJournal of Experimental & Clinical Cancer Research誌、Cancers誌及びCell Death Discovery誌に掲載された。 カイオム・バイオサイエンスでは、CBA-1535の次世代型パイプラインとして、今後の開発・導出に注力する考えだ。 |
PXLR(ヒト化抗CXCL1/2/3/5抗体) | |
概要 | CXCR2発現細胞の走化性因子であるCXCL1/2/3/5の機能阻害抗体であり、薬剤耐性のがん微 小環境を改善させるがん治療抗体 |
想定適応疾患 | 固形がん(胃がん、乳がん、卵巣がん、など) |
期待 | がん細胞はCXCL1/2/3/5を発現し、薬剤耐性環境の原因細胞である免疫抑制細胞を呼び寄せ る。PXLR抗体の投与により免疫抑制細胞を減少させ、薬剤耐性を克服およびがんの再発抑 制が期待される。 |
知財 | 特許出願を完了 |
開発の進捗 | 非臨床試験中。大阪公立大学との共同研究を進めている。 |
BMAA(ヒト化抗セマフォリン3Aモノクローナル抗体)、LIV-2008/2008b(ヒト化抗TROP-2モノクローナル抗体)、創薬研究プロジェクト等、他のパイプラインについては、引き続き成果創出に向けて取り組み、適宜進捗を報告することとしている。
※ADC抗体
抗体薬物複合体。悪性腫瘍や炎症性疾患等の目的の組織や細胞表面タンパク質(抗原)に特異的に結合する抗体に抗がん剤などの薬物を結合させることにより、薬剤を病変部位に選択的に到達させ、細胞内に放出させることでがん細胞等を死滅させることができる。
※Tribody®技術
3つの異なる抗原結合部位を持つ抗体を創製する技術で、複数の抗原に結合することができる多重特異性や腫瘍細胞を攻撃するT細胞誘導活性を有する抗体(multispecific T-cell engager antibody)を創り出すことができる。
(2)創薬支援事業
製薬企業、診断薬企業および大学等の研究機関で実施される創薬研究を支援することで、契約一時金、マイルストーン、ロイヤルティ、受託サービス料等の対価を獲得する事業。主として国内製薬大手企業に対して、同社の保有する抗体創薬技術プラットフォームを活用した抗体作製・抗体エンジニアリングおよびタンパク質調製を提供する「高付加価値型受託研究ビジネス」であり、安定的な収益獲得を目的としている。
(主なサービスの内容)
サービス項目 | 内容 |
タンパク質・抗原調製、抗体の発現精製 | 抗体作製に必要な組換えタンパク質(抗原)や、研究開発用途の抗体などを細胞に発現させ、精製を行う。 種類に応じた発現・精製方法を選び、純度や物性の分析を行う。 |
安定発現細胞株作製 | 安定的に組換えタンパク質(抗原や抗体)を供給できるように、遺伝子組換え技術を用いて、組換えタンパク質を効率よく発現する細胞株を作製する。 |
ADLib®システムによる抗体作製 | ADLib®システムによる抗体作製技術を用い、創薬研究に用いるモノクローナル抗体作製を行う。同社の抗体作製の知識・ノウハウを活かし、顧客のニーズに合わせた抗体作製プランを提案する。 |
ADLib®システムを用いた抗体の親和性向上業務 | 同社が培ったADLib®システムの技術・ノウハウを活かし抗体の結合力(抗体親和性)を向上させることで、より薬効の高い抗体医薬の精製が期待できる。 |
中外製薬株式会社および同社の海外子会社であるChugai Pharmabody Research Pte. Ltd.の「中外製薬グループ」からの委託研究、小野薬品工業や協和キリンとの委託研究など、抗体医薬の研究開発を進める国内製薬企業との抗体作製プロジェクトなどを手掛けている。
取引先名称 | 契約締結年月 |
・中外製薬株式会社 | 2011年6月 |
・ChugaiPharmabodyResearch Pte.Ltd | 2012年8月 |
・田辺三菱製薬 | 2016年12月 |
・小野薬品工業株式会社 | 2018年10月 |
・協和キリン株式会社 | 2019年7月 |
・武田薬品工業株式会社 | 2024年2月 |
このほか、販売提携契約をメルク株式会社(契約締結2024年9月)、富士フイルム和光純薬株式会社(同2024年12月)と締結している。今後も同社技術の品質の高さを理解し、長期的・安定的な付き合いが可能な新規契約先獲得を目指している。
(3)新規事業
創薬事業、創薬支援事業に加え、新たに立ち上げたのが「IDDビジネス」である。またその一環として「バイオシミラー医薬品事業」にも注力している。
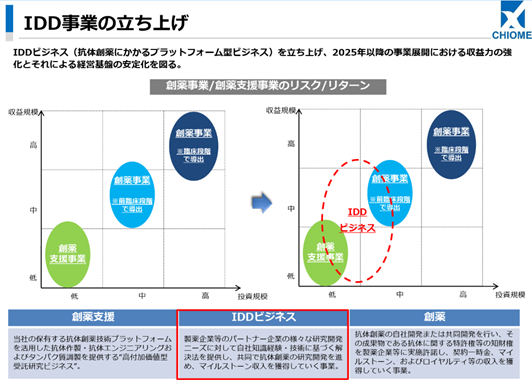
【IDD(Integrated Drug Discovery)ビジネス】
①IDDビジネスの概要
IDDビジネスとは、抗体創薬にかかるプラットフォーム型ビジネス。
抗体創薬のプロジェクトにおいてスクリーニング、in vitro/vivo評価(※)、CMC(※)、IND(Investigational New Drug Application、新薬臨床試験開始申請)、初期臨床までを一気通貫で対応可能なプラットフォームを構築し、製薬企業等のパートナー企業の様々な研究開発ニーズに対して自社の知識・経験・技術に基づく解決法を提供し、共同で抗体創薬の研究開発を進め、マイルストーン収入などによりマネタイズする。
製薬会社は、モダリティ(製薬の基盤技術の方法・手段)が多様化する中で、個別モダリティの専門性の維持確保が困難になっている。また、スタートアップは、適切な開発ステップの実行能力を各社で個別に整える事には限界がある。
このように、抗体創薬研究を推進するにあたり専門性やリソースが不足しているため未着手となっているケースは多く、同社の知識経験を用いて有望な抗体創薬研究に関するコラボを推進することは大きな需要を取り込むことができると同社では考えている。
※in vitro/vivo評価
in vitro(試験管内・細胞)評価は細胞や組織を用いた実験室レベルの基礎・スクリーニング試験。in vivo(生体内・動物)評価はマウス等の生体を用いた包括的な薬効・安全性試験。
※CMC
新薬候補の物質(原薬)を、安定した品質で製造し、安定供給するための技術・管理(化学、製造、品質管理)を指す。製剤処方開発、分析法確立、包装設計、スケールアップ生産などが含まれ、創薬と製造の架け橋となる重要な部門。
②IDDビジネスの進捗
2024年12月に、エーザイ株式会社との間で、ADLib®システムを応用した抗体エンジニアリングによる高親和性抗体の作製について、共同研究契約を締結した。
抗体エンジニアリングは、単離した抗体の機能を目的に沿った形で高機能化する工程であり、抗体作製過程においては重要性の高い技術である。ADLib®システムは、標的に対する抗体を取得することのほか、抗体遺伝子に変異を蓄積させる性質を応用した抗体の高機能化をこれまでの研究において実証しており、今回の共同研究は、エーザイの抗体創製技術と、カイオム・バイオサイエンスの抗体エンジニアリング技術を活かし、高機能な抗体を創製することを目指すもので、IDDビジネスの一例となる。2025年12月、良好かつ発展的な結果を得たことから、共同研究契約を延長することとなった。
2025年3月には、医薬品の開発支援を行う 株式会社エスアールディ(SRD社)と医薬品開発に関する業務提携契約を締結した。SRD社は本業の CRO(開発業務受託機関)事業領域以外で、長年培ってきた幅広い分野での臨床研究・開発支援に関するノウハウを用いた創薬ベンチャー支援事業も行っている。カイオム・バイオサイエンスは、バイオベンチャーが臨床開発を進める上で必要となる経験・ノウハウを生かし、SRD 社が実施する創薬ベンチャー支援において、非臨床開発の戦略立案、製剤化に関する計画立案、First in human試験及びPOC 試験実施に向けた臨床開発の戦略立案のコンサルティングを行う。SRD社の創薬ベンチャー育成事業に参画することで、新たな創薬ベンチャー育成に関するコンサルティング等に対する対価を受領することとなっている。
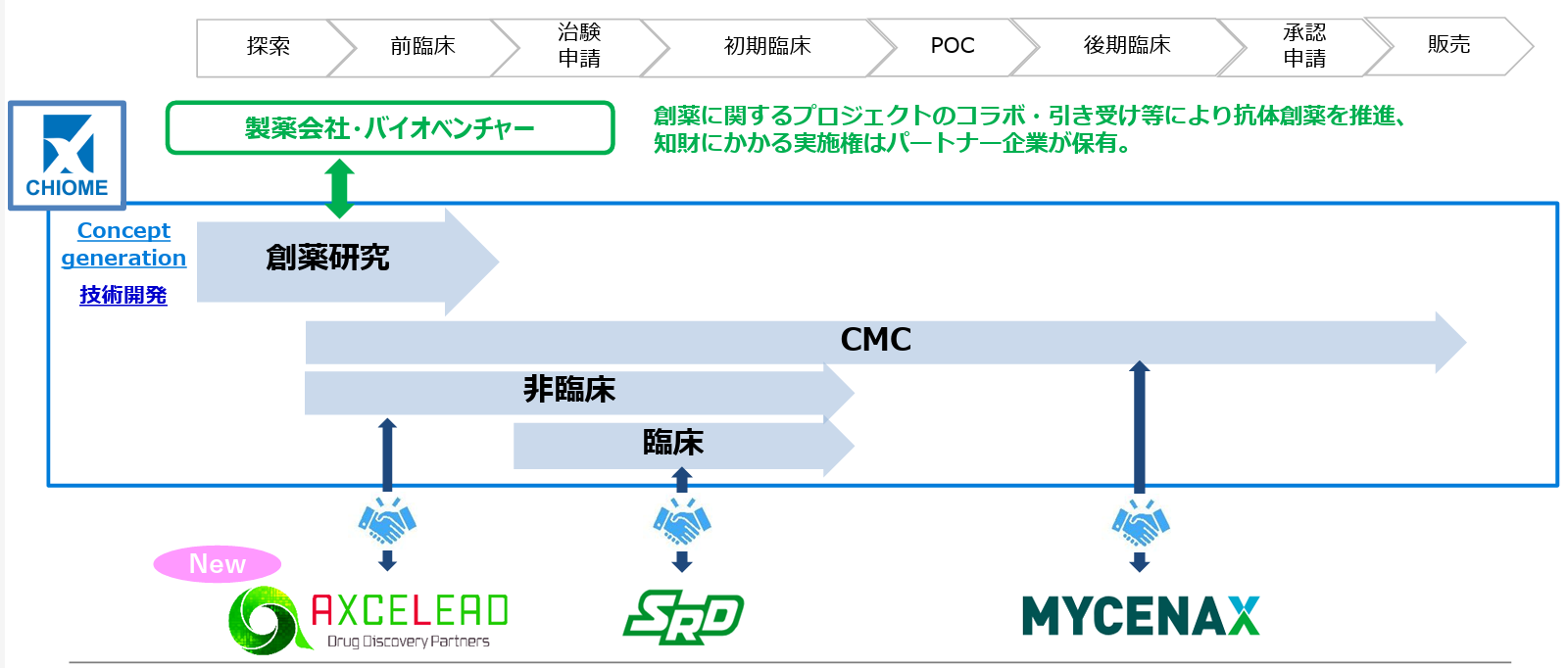
2025年10月には、Axcelead Drug Discovery Partners株式会社(Axcelead DDP)、 と、IDDビジネスの協業に関する業務協力基本合意書を締結した。Axcelead DDPは、創薬ソリューションプロバイダーのパイオニアで、武田薬品工業株式会社の創薬プラットフォームを元に幅広い創薬モダリティでIDD事業の実績を有する企業。カイオムバイオサイエンスの Biologics における強みとAxcelead DDPの幅広い評価プラットフォームの強みを組み合わせることにより、製薬会社やバイオベンチャー等の創薬研究機関における創薬ニーズを広く汲み上げ、創薬課題解決のためのソリューションの提供を推し進める事により、日本の創薬力強化への貢献を目指す。
今回のAxcelead DDPとの業務提携により、初期臨床から承認申請・販売に至る領域も幅広くカバーできることとなった。シーズの発掘のための国内外のベンチャーキャピタルとの連携も進め、コンソーシアム型スタートアップインキュベーション体制を一段と強化する。カイオム・バイオサイエンスは「ものづくり」の面からバイオ産業における探索及びCMC開発機能を提供していく。
 |
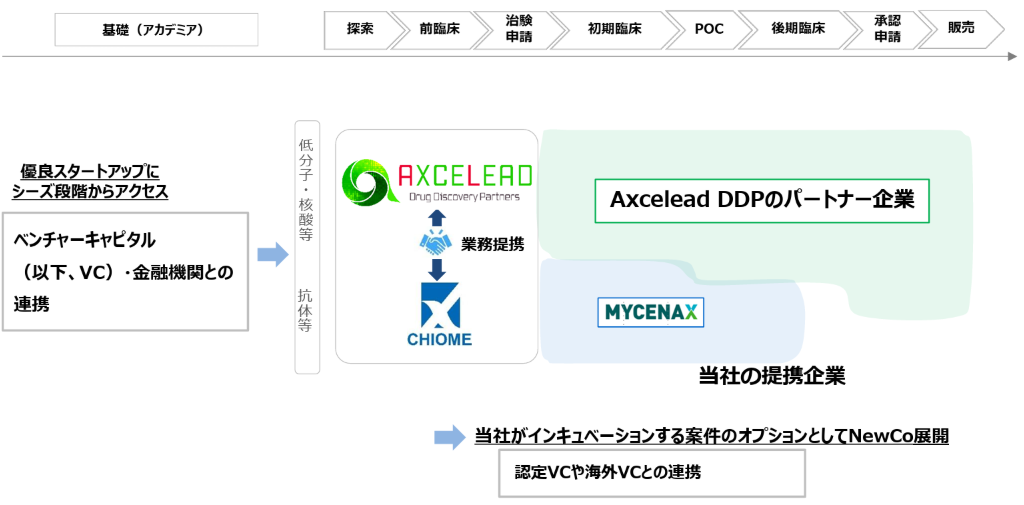 |
(同社資料より)
同事業はリスク・リターンの面からは、創薬支援事業と前臨床段階での導出を行う創薬事業の中間に位置し、2025年以降の事業展開における収益力の強化とそれによる経営基盤の安定化に資するものと位置付けている。
(同社資料より)
【バイオシミラー医薬品事業】
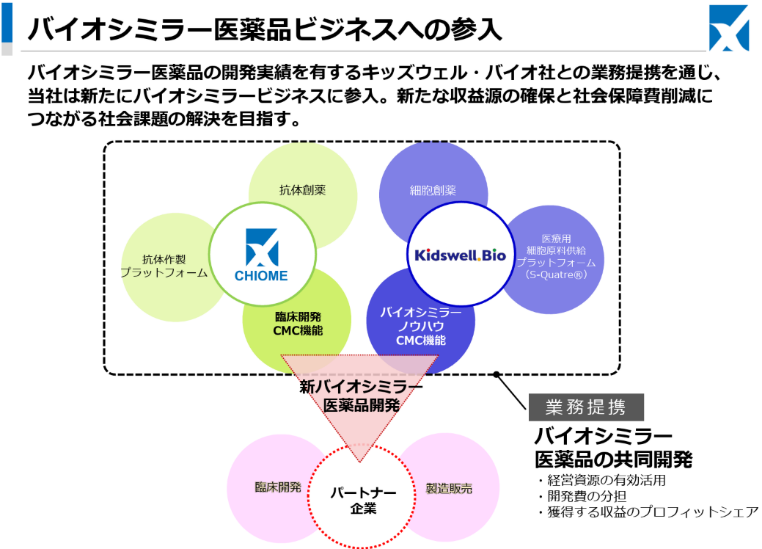
24年6月、バイオシミラー医薬品の開発実績を有するキッズウェル・バイオ株式会社との業務提携を通じ、新たにバイオシミラー医薬品開発に参入すると発表した。
(バイオシミラー医薬品とは?)
既に承認・販売されているバイオ医薬品(先行バイオ医薬品)の特許期間・再審査期間満了後に、異なるメーカーから販売される、先行バイオ医薬品と同等/同質、安全性および有効性を有する医薬品。
分子サイズが小さく、化学合成によって先行品と完全に同一である製品を製造することが可能な「後発医薬品 (ジェネリック医薬品)」に対し、バイオ医薬品は、分子サイズが大きく、構造が複雑なため、製造業者が異なることによる製造工程の違いの影響をうけやすく、先行品と完全な同一品を製造することは困難なため、同等性/同質性を証明するために、新薬に準ずる様々な試験(品質試験、薬理試験、毒性試験、臨床試験など)が必要である。薬価は原則として先行バイオ医薬品の 70%に設定されるため、患者の経済的負担や医療費の軽減が期待される。
(キッズウェル・バイオ株式会社概要)
2001年設立。「バイオで価値を創造する-こども・家族・社会をつつむケアを目指して-」を企業理念に掲げ、既にバイオシミラー医薬品4製品を上市し安定的な収益基盤であるバイオシミラー事業と、臨床開発ステージに入り今後の飛躍的な成長基盤として期待される細胞治療事業(再生医療)を推進している。病気に苦しむ患者、特に子供たちに、革新的な治療薬・治療法を提供し、明るく幸せに暮らすことができる社会の実現に貢献すべく、日々研究開発活動に取り組んでいる。
(同事業参入の意義)
同社がこれまでに取り組んでいる新薬開発は長期にわたって研究開発投資を行うハイリスク・ハイリターン型のビジネスモデルであり、新薬開発に必要な研究開発資金を、抗体創薬プラットフォームを活かした安定的な収益を獲得する創薬支援事業とエクイティファイナンスを中心とした資金調達によって賄っている。同社の技術基盤を活かした創薬支援事業についてはこれまでに継続的にその取引規模を拡大してきたが、一方で、目下の株式市場の環境や長期金利の動向は不確実性を増しており、資金調達環境は変化している。
バイオシミラー医薬品は社会保障費の適正化と医薬品の安定供給に向けて、厚生労働省によるバイオシミラーの普及目標の設定、バイオシミラーの使用促進に向けた診療報酬の新設等、その積極的な開発と普及が期待される薬剤であり、新薬開発よりも開発投資額が抑えられ成功確度を高く見込むことができる。同社の新薬開発チームにはバイオシミラー医薬品の開発・上市経験を有するメンバーが在籍しているが、バイオシミラービジネスで既に4製品の承認品目を有するキッズウェル・バイオ社との提携によって、新たにバイオシミラー医薬品ビジネスに参入し、新薬開発と製薬会社の研究支援に続く第三の収益源創出、および社会課題の解決を行うことを目的としている。
(事業展開の進捗)
◎厚生労働省「バイオ後続品国内製造施設整備支援事業」の助成対象事業者に採択
厚生労働省の「バイオ後続品国内製造施設整備支援事業」に、アルフレッサホールディングス、キッズウェル・バイオ、カイオム・バイオサイエンスの3社で共同申請を行い、2025年5月、助成対象事業者に採択された。
*助成事業の概要
日本国内でバイオ後続品を安心して使用できる環境整備を目的に、厚生労働省が製造施設の整備から安定的な製造・供給までを行うに十分なノウハウ、人材、経営基盤等を有する事業者を選定し、補助を行うもの。
*助成事業への採択の経緯
バイオシミラー医薬品の開発実績を有するキッズウェル・バイオ株式会社との業務提携に続き、バイオシミラー医薬品のさらなる普及と安定供給体制の確立、バイオ医薬品の製造を通じたバイオ人材の育成が日本国内における重要な課題であるとの認識のもと、バイオシミラー製品の国内製造拠点の必要性について、アルフレッサ ホールディングス、キッズウェルと協議を進め、同事業の推進に関する意義について合意し、同助成事業への共同申請を行った。
加えて、台湾においてバイオシミラーを含むバイオ医薬品の受託開発製造機関として多くの経験を有し、近年自社製造施設の整備経験を有する、Mycenax Biotech Inc.(MBI社)を含めた4社で協働関係を構築し、今後の具体的な製造設備の整備に向けて詳細な連携を図ることとした。
*助成事業における各社の協働概要
今後の具体的な活動は、日本国内に、バイオシミラーを商用スケール規模で製造(原薬及び製剤)することができる施設を建設・整備し、稼働させること。同助成事業の採択に伴い、今後は申請における活動方針に基づき各社の役割を明確化した契約締結を経て、業務を推進する。4社がそれぞれの強みを活かし、製造施設を整備し、バイオシミラーの開発から製造、流通までを含む供給プロセスの一貫したトータルバリューチェーンを構築する。
カイオム・バイオサイエンスは主として新規バイオシミラー医薬品の開発を担うこととなっており、新施設での製造を視野に入れた新たなバイオシミラー医薬品開発を推進する。

(同社資料より)
◎バイオシミラー医薬品の原薬・製剤製造を行う合弁会社を設立
2025年10月、上記助成事業を推進するため、カイオム・バイオサイエンス、アルフレッサ ホールディングス、キッズウェル、MBIの4社は、バイオシミラー医薬品の国内製造施設となる合弁会社「Alfenax Biologics 株式会社(アルフェナックス バイオロジクス)」を設立することを基本合意した。出資比率はアルフレッサ ホールディングス45%、MBI45%、キッズウェル7%、カイオム・バイオサイエンス3%。設立年月日は現時点では未定。
製造施設はアルフレッサ ホールディングスの子会社であるアルフレッサ ファインケミカル株式会社(秋田県秋田市)の敷地内に建設することで準備を進めている。
製造施設の整備完了後、新規バイオシミラー医薬品の製造をこの製造施設に移管することを想定しており、現在の委託先であるMBIと連携することで、スムーズな技術移管と稼働、バイオシミラー医薬品の安定供給体制構築を実現する。
合弁会社設立により、新規開発から製造・供給までをカバーする国内初のバイオシミラー医薬品のサプライチェーン構築と安定供給の実現に向けた取り組みをさらに推進する考えだ。
◎バイオシミラー医薬品開発に関する基本合意書と個別製品の共同開発のための基本契約書を締結
上記合弁会社設立のリリースと同日、カイオム・バイオサイエンス、アルフレッサ ホールディングス、キッズウェルの3社で、バイオシミラー医薬品開発に関する基本合意書と個別製品の共同開発のための基本契約書を締結したと発表した。
抗体医薬の研究開発に長年の経験を有するカイオム・バイオサイエンス、医薬品等製造事業を有し、医療用医薬品等卸売事業において国内に医薬品等の全国流通ネットワークを構築しているアルフレッサグループ、複数のバイオシミラーの製品開発と安定供給に携わるキッズウェルのそれぞれの強みを生かし、新規バイオシミラー医薬品創出に向けた協業を進める。開発された新規バイオシミラー医薬品については、厚生労働省の助成事業で整備する国内製造施設へ移管し商用製造し、製造実績の積み上げと同施設の安定操業を目指す。
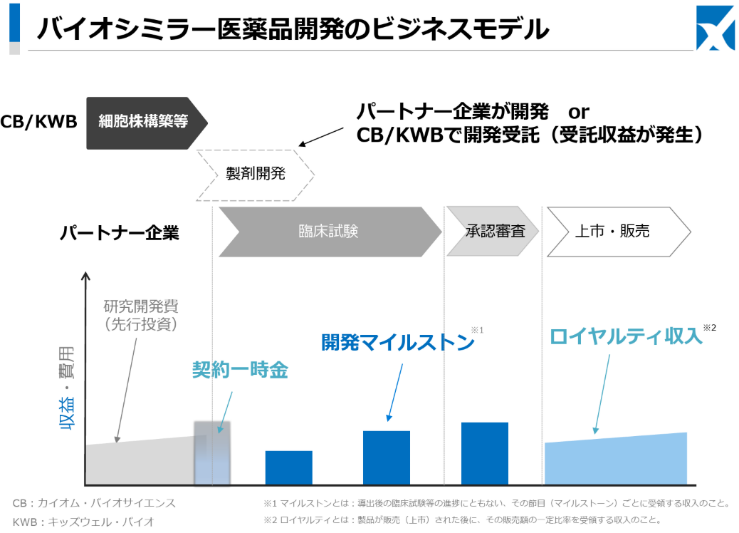
(ビジネスモデル)
同社とキッズウェル・バイオ社が先行投資によって細胞株構築等を行った後の製剤開発ステージにおいては、導出先のパートナー企業が自ら開発を行う、もしくは、同社とキッズウェル・バイオ社が開発を受託するケースを想定している。現在、パートナー企業の選定と協業交渉を行っている。
収益は、製剤開発スタート時の「契約一時金」、導出後の臨床試験等の進捗に伴ってその節目(マイルストーン)ごとに受領する収入である「開発マイルストン」、製品が販売(上市)された後に、その販売額の一定比率を受領する収入である「ロイヤルティ収入」となる。
 |
 |
(同社資料より)
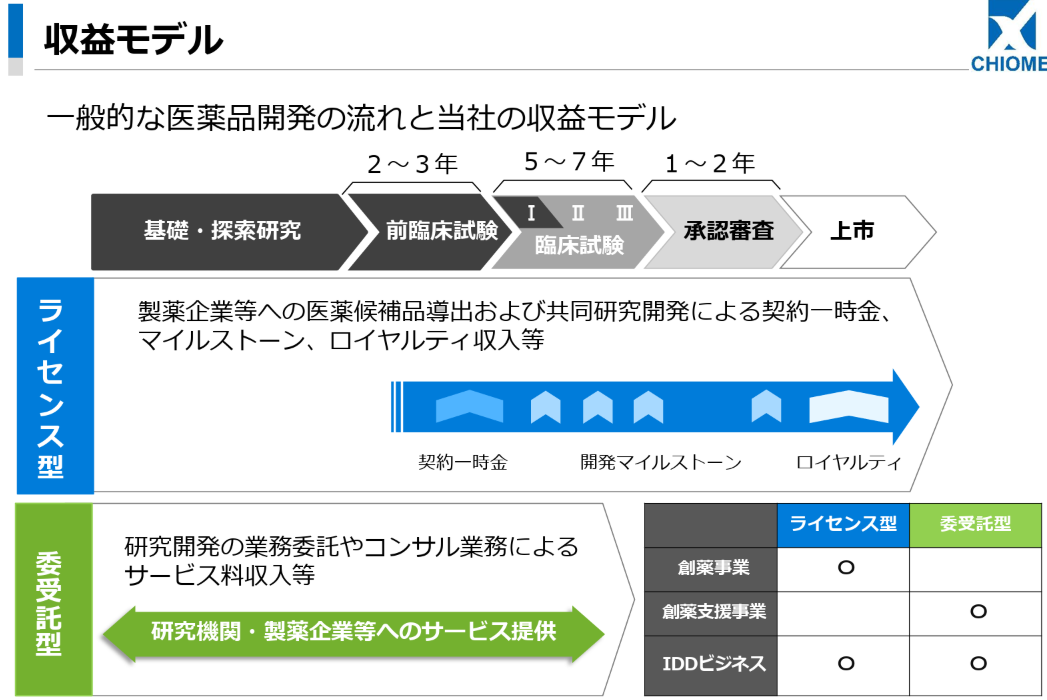
【1-5 収益モデル】
これまでは、創薬事業における製薬企業等への医薬候補品導出および共同研究開発による契約一時金、マイルストーン、ロイヤルティ収入等「ライセンス型」収益と、創薬支援事業における研究開発の業務委託やコンサル業務によるサービス料収入「委受託型」収益であったが、IDDビジネスは「ライセンス型」「委受託型」双方の収益モデルを有しており、収益源の多様化が進むこととなる。
【1-6 特長と強み】
(1)高い抗体開発候補品創出能力
同社では以下の3点から構成される抗体開発候補品創出能力が成長の源泉であると考えている。この優位性を活かし、ベンチャーならではのアジャイル型研究開発体制により、最小の工数や資金で効率的な投資判断を行い、最大のリターンを狙っている。
①複数の抗体作製技術と技術プラットフォーム
医薬品候補抗体を継続的に創出するための独自の「ADLib®システム」をはじめとして、Tribody®、ハイブリドーマ法、DNA免疫法、細胞免疫法、タンパク質調整など、複数の抗体作製技術、タンパク質調製や抗体エンジニアリングに関する技術やノウハウ等からなる技術プラットフォームを保有している。
②医薬品候補の創製から初期臨床開発まで最速で実施できる体制
臨床開発機能を有し、自社による創薬テーマの設定から前臨床パッケージの構築、開発戦略および薬事戦略の立案、ならびにCMC開発によるCMOマネジメントなど、医薬品候補の創製から初期臨床開発までを最速で実施できる体制を確立している。
③研究開発を遂行する優秀な人材
開発メンバーの多くは上市を経験している。また、博士号を持つ研究者を多数有している。
こうした専門性の高い人材が持つネットワークを通じて、研究開発の推進に最適なリソースや資源を獲得することが可能である。
(2)創薬ビジネスにおいて独自のポジションの確立へ
大手製薬会社などは、がん領域、中枢神経領域など、領域を絞り込んで抗体作製に取り組むのが一般的である。また、国内外のバイオベンチャー等が研究開発を進めてきた開発候補品を外部から導入するケースが増えている。他方では医療用医薬品開発においてはアンメットメディカルニーズが依然として多く存在しており、今後の治療薬の開発が待たれている。
これに対し同社は、アンメットニーズで創薬の可能性のあるターゲットであれば領域を限定せず早期の段階から抗体作製に取り組み、複数の製薬会社を導出候補として医薬品のライセンスビジネスに取り組んでいる。
アンメットニーズに対する新規プロジェクトを継続的に立ち上げ、技術ポートフォリオを統合的に活用し探索プロジェクトの回転を速くすることで、できるだけ多くの開発候補品を創出するという、独自のポジションを確立しようとしている。
また、欧米では創薬のプロセスにおいてシーズを提供するアカデミアと製品化を目指すメガ・ファーマをつなぐ役割としてバイオベンチャーが重要な役割を果たしており、創薬のエコシステム(※)が機能しているが、日本では未成熟である。
同社では、抗体開発候補品創出能力の高さを武器に日本の創薬エコシステムにおいてなくてはならないポジションを確保することで勝機を見出そうとも考えている。
※エコシステム
本来の意味である生態系に端を発し、複数の企業によって構築された、製品やサービスを取り巻く共通の収益環境。この場合、欧米においては創薬に関わる全企業に収益をもたらす環境が構築されていることを意味する。
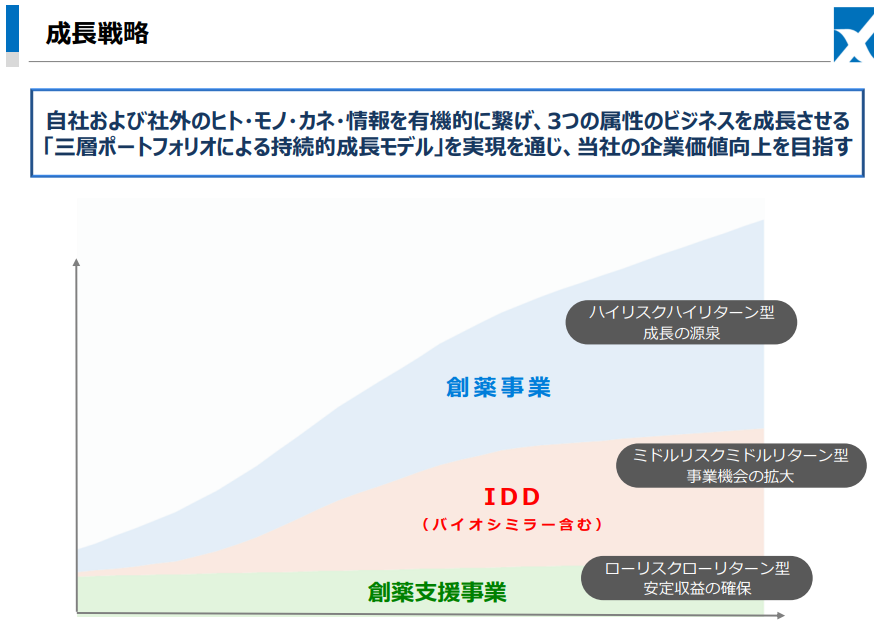
【1-6 成長戦略】
技術プラットフォームをコアとし、高品質な研究支援機能を提供する「創薬支援事業」の安定した収益の獲得をベースに、アンメットニーズに対する抗体医薬品候補を複数創製し、製品価値の増大や導出による事業化に注力する。
エクイティによる資金調達に過度に依存しない経営を目指し、インテリジェンスを活かした新事業であるIDDビジネスやバイオシミラー事業を推進することで収益性を高め、経営の安定化および企業価値の増大を図る考えだ。
(同社資料より)
2.2025年12月期算概要
(1)業績概要
| 24/12期 | 構成比 | 25/12期 | 構成比 | 前期比 | |
売上高 | 780 | 100.0% | 593 | 100.0% | -187 | -24.0% |
売上総利益 | 432 | 55.4% | 355 | 59.9% | -77 | -17.9% |
販管費 | 1,463 | 187.5% | 1,335 | 225.1% | -128 | -8.8% |
うち、研究開発費 | 936 | 120.0% | 776 | 130.9% | -160 | -17.1% |
営業利益 | -1,030 | - | -979 | - | +51 | - |
経常利益 | -1,019 | - | -989 | - | +30 | - |
中間純利益 | -1,020 | - | -982 | - | +37 | - |
*単位:百万円
減収、損失幅縮小
売上高は前期比24.0%減(1億87百万円減)の5億93百万円。創薬支援事業は増収。営業損失は同51百万円縮小の9億79百万円。研究開発費が同1億60百万円減少した。主に治験薬製造費用等の減少によるものである。
(2)セグメント別動向
| 24/12期 | 25/12期 | 前期比 | |
創薬事業 | 202 | - | -202 | -100.0% |
創薬支援事業 | 577 | 593 | +15 | +2.7% |
連結売上高 | 780 | 593 | -187 | -24.0% |
創薬事業 | -813 | -776 | +37 | - |
創薬支援事業 | 309 | 355 | +45 | +14.7% |
調整額 | -526 | -558 | - | - |
連結営業利益 | -1,030 | -979 | +51 | - |
*単位:百万円
◎創薬事業
売上高は計上されなかった。前期は旭化成ファーマ株式会社とのライセンス契約締結により受領した契約一時金の計上があった。営業損失は前期比37百万円改善の7億76百万円。研究開発費は同1億60百万円減の7億76百万円。
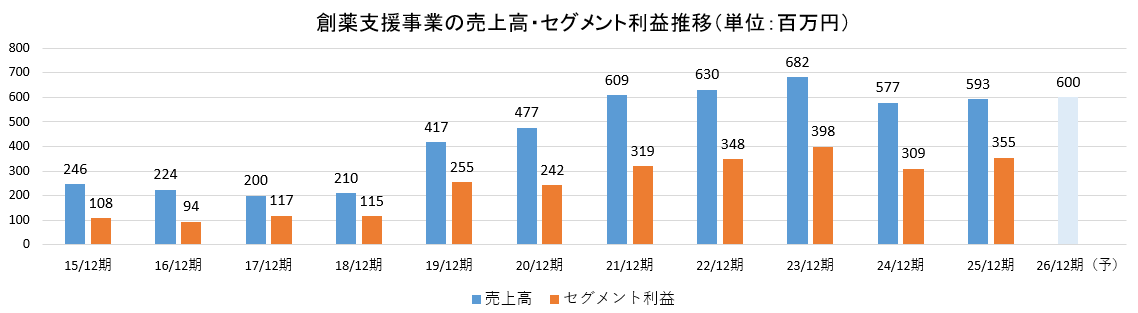
◎創薬支援事業
売上高は前期比15百万円増の5億93百万円。5億円としていた期初予想を上回った。主にアルフレッサ ホールディングス株式会社とのバイオシミラー医薬品の共同開発契約締結に伴う収益を計上したことによるもの。
営業利益は同45百万円増の3億55百万円。抗体創薬の技術・サービスは高い評価を得ており、既存顧客との取引は安定的に推移。日東紡績株式会社等、複数の新規顧客獲得も進んだ。引き続き収益基盤安定化のために取り組んでいる。
(3)財政状態とキャッシュ・フロー
◎主要BS
| 24/12末 | 25/12末 | 増減 |
| 24/12末 | 25/12末 | 増減 |
流動資産 | 2,337 | 1,546 | -790 | 流動負債 | 493 | 374 | -118 |
現預金 | 2,063 | 1,205 | -858 | 短期借入金 | 281 | 86 | -194 |
売掛金 | 51 | 71 | +20 | 固定負債 | 55 | 230 | +175 |
固定資産 | 131 | 180 | +49 | 負債合計 | 548 | 605 | +56 |
有形固定資産 | 0 | 36 | +36 | 純資産 | 1,920 | 1,122 | -798 |
投資その他の資産 | 131 | 144 | +13 | 利益剰余金 | -1,020 | -2,003 | -982 |
資産合計 | 2,468 | 1,727 | -741 | 負債純資産 | 2,468 | 1,727 | -741 |
*単位:百万円
現預金の減少などで資産合計は前期比7億41百万円減の17億27百万円。
負債合計は同56百万円増の6億5百万円。
利益剰余金の減少などで、純資産は同7億98百万円減少し11億22百万円。
自己資本比率は前期末から13.3ポイント低下して64.1%となった。
◎キャッシュ・フロー
| 24/12期 | 25/12期 | 増減 |
営業CF | -1,000 | -935 | +64 |
投資CF | - | -55 | -55 |
フリーCF | -1,000 | -991 | +9 |
財務CF | 1,738 | 133 | -1,605 |
現金及び現金同等物 | 2,063 | 1,205 | -858 |
*単位:百万円
株式の発行による収入の減少で財務CFのプラス幅は縮小。キャッシュポジションは低下した。
(4)トピックス
①創薬事業
*CBA-1205
第1相試験では肝細胞がん、メラノーマに加え、小児がんパートを追加し、症例登録を開始した。
*CBA-1535
第1相試験では単剤パートのデータのみでの早期導出等の可能性も見据え、プロトコルを改訂し、プレメディケーション(前投薬)を実施した上で投与用量の増量中である。
※【1-4 事業内容:創薬事業 主要パイプラインおよび開発状況】を参照。
②創薬支援事業
アルフレッサ ホールディングス株式会社とのバイオシミラー医薬品の共同開発契約締結に伴う収益を計上した。
③新規事業
*IDDビジネス
Axcelead Drug Discovery Partners株式会社(Axcelead DDP)、 と、IDDビジネスの協業に関する業務協力基本合意書を締結。※【1-4 事業内容:新規事業 IDDビジネス】を参照。
*バイオシミラー医薬品事業
・バイオシミラー医薬品の原薬・製剤製造を行う合弁会社を設立
・バイオシミラー医薬品開発に関する基本合意書と個別製品の共同開発のための基本契約書を締結
※【1-4 事業内容:新規事業 バイオシミラー医薬品事業】を参照。
⑤新規技術開発
2025年8月、カイオム・バイオサイエンスのTribody®技術を始めとする最先端の抗体創薬技術と、NANO ホールディングス株式会社(東証グロース、4571)のmRNA創薬基盤技術の融合によるmRNAエンコード抗体の創出に向けた共同研究契約を締結した。
この共同研究では、1年以内を目途に開発候補品を選定し、その後、開発候補品のin vivoでのデータ取得と物性面での最適化を経て知財化、および製薬企業との共同開発或いは導出を目指す。mRNAエンコード抗体は、抗体のmRNAを投与し、体内で目的の抗体を産生させるという次世代の抗体医薬モダリティ。既存の技術に比べ、体内動態改善とそれに伴う効果の増強、副作用の軽減に加え、製造コストの削減や製造期間の短縮も期待され、世界的に注目されている。海外では既にModerna社、BioNTech社などが臨床開発を開始しており、BioNTech社のClaudin 6-CD3 bi-specific mRNAエンコード抗体BNTについては、半減期が大幅に伸びるなど優れた薬物動態プロファイルと顕著な薬効を示すことが発表され、革新的な医薬品技術になることが期待されている。
3.2026年12月期の見通し
創薬事業における合理的な業績予想の算定が困難なため、2026年12月期の業績予想は創薬支援事業の売上高6億円のみ開示している。
(1)創薬事業
CBA-1205及びCBA-1535の第1相試験の終了に向けた着実な進展を目指すとともに、臨床2品目や非臨床段階のパイプラインを含めた導出候補品の導出活動、二重特異性抗体作製技術や創薬ノウハウを用いた製薬会社とのコラボレーションを推進する。
*CBA-1205
臨床第1相試験は2026年内に肝細胞がん患者及び小児がん患者の登録終了を目標として後半パートが進行中。今後の導出活動において重要となる肝細胞がん患者、メラノーマ患者並びに小児がん患者での安全性及び初期の有効性の評価を進めていく。複数の癌腫において薬効が確認された場合、導出活動を有利に進めることができるため、その可能性を追求した臨床開発を推進する。
*CBA-1535
前半パートの治験結果からの導出等の可能性を見据えて、2026年内での前半パート終了を目指す。
*IDDビジネス
自社のBiologics領域での創薬知見・技術を生かし、製薬会社やバイオベンチャー等の創薬ニーズの課題解決のためのソリューションを提供すべく、複数社との間で業務提携契約および業務委託契約を締結するなどの収益化に向けたビジネス基盤の構築を進めている。また、二重特異性抗体のハイスループットスクリーニング手法の「DoppeLib™」等も用いながら、2025年度に構築したビジネス基盤を通じて新薬開発やスタートアップ支援等を推進し、今後の収益獲得を進める。
*バイオシミラービジネス
共同開発下での細胞株構築を継続し、2026年度以降の開発業務及び開発パートナー獲得を目指した活動を推進する。
(2)創薬支援事業
売上高は前期比1.1%増の6億円を見込んでいる。技術サービス力を活用し既存顧客ニーズに対して丁寧に対応するとともに、業務提携契約にもとづく拡販体制を活用するなどして、安定的な収益基盤として抗体作製やタンパク質調製等の受託業務を推進する。IDDビジネスやバイオシミラービジネスにおける新薬開発やバイオシミラー開発から獲得する収益の拡大を企図した活動も並行して取り組んでいく。
5.今後の注目点
バイオシミラー医薬品開発に伴う収益を計上したことも寄与し、減収を見込んでいた創薬支援偉業は小幅ではあるが増収となった。新規顧客開拓も進んでいるようで、収益基盤強化が進んでいる。
リスク・リターンの面からは、創薬支援事業と前臨床段階での導出を行う創薬事業の中間に位置し、2025年以降の事業展開における収益力の強化とそれによる経営基盤の安定化に資するものと位置付けるIDDビジネスも、バイオシミラー医薬品事業とともに着実に進捗を示している。中心的な開発品である「CBA-1205」「CBA-1535」におけるライセンス契約の獲得動向とともに、引き続き各事業の進捗に注目していきたい。
<参考:コーポレートガバナンスについて>
◎組織形態、取締役、監査役の構成
組織形態 | 監査等委員会設置会社 |
取締役 | 7名、うち社外4名(うち独立役員2名) |
監査等委員 | 3名、うち社外取締役3名(うち独立役員3名) |
◎コーポレートガバナンス報告書
最終更新日:2025年8月13日
<基本的な考え方>
当社は、ライフサイエンスを通じて持続的な成長と企業価値の向上を図るとともに、株主、顧客をはじめ、取引先、研究パートナー、地域社会、従業員等の全てのステークホルダーに対してフェアな企業であることを目指しております。そのためには、コンプライアンスの徹底、経営活動の透明性の向上、責任の明確化に努めていくことを重要な課題と捉え、コーポレートガバナンスの継続的な充実に取り組んでまいります。
<コーポレートガバナンス・コードの各原則を実施しない理由>
当社はコーポレートガバナンス・コードの【基本原則】をすべて実施しております。
本レポートは、情報提供を目的としたものであり、投資活動を勧誘又は誘引を意図するものではなく、投資等についてのいかなる助言をも提供するものではありません。また、本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、当社は、本レポートに掲載されている情報又は見解の正確性、完全性又は妥当性について保証するものではなく、また、本レポート及び本レポートから得た情報を利用したことにより発生するいかなる費用又は損害等の一切についても責任を負うものではありません。本レポートに関する一切の権利は、当社に帰属します。なお、本レポートの内容等につきましては今後予告無く変更される場合があります。投資にあたっての決定は、ご自身の判断でなされますようお願い申し上げます。 Copyright(C) Investment Bridge Co., Ltd. All Rights Reserved. |
ブリッジレポート(カイオム・バイオサイエンス:4583)のバックナンバー及びブリッジサロン(IRセミナー)の内容は、www.bridge-salon.jp/ でご覧になれます。
 | 同社の適時開示情報の他、レポート発行時にメールでお知らせいたします。 |
 | ブリッジレポートが掲載されているブリッジサロンに会員登録頂くと、株式投資に役立つ様々な便利機能をご利用いただけます。 |
 | 投資家向けIRセミナー「ブリッジサロン」にお越しいただくと、様々な企業トップに出逢うことができます。 |


